
科目: 来源: 题型:
(10分)下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,A是具有刺激性气味的气体,I是由地壳中含量最高的金属元素形成的单质,K是一种红棕色气体,D是一种红棕色粉末,常用作红色油漆和涂料。
![]()
 |
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
请填写下列空白:
⑴在周期表中,组成单质G的元素位于第______周期______族。
⑵在反应⑨中还原剂与氧化剂的物质的量之比为______________。
⑶在反应②、③、⑥、⑧中,既属于化合反应又属于氧化还原反应的是_________(填写序号)。
⑷反应④的离子方程式是:_________________________________。
⑸将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:_____________________。
查看答案和解析>>
科目: 来源: 题型:
(10分)沉淀物并非绝对不溶,其在水及各种不同的溶液中溶解有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。下图是AgCl在NaCl、AgNO3 溶液中的溶解情况。

由以上信息可知:
(1)AgCl的溶度积常数的表达式为: ,由图知AgCl的溶度积常数为 。
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
![]()
(3)反应AgCl + KI== AgI + KCl能在水溶液中进行,是因为 。
(4)若在AgCl形成的浊液中滴加氨水有什么现象?
![]() 发生反应的离子方程式为 .
发生反应的离子方程式为 .
查看答案和解析>>
科目: 来源: 题型:
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列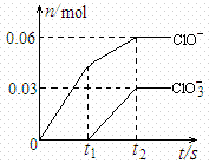 说法正确的是
说法正确的是
A.苛性钾溶液中KOH的质量是4.94g
B.反应中转移电子的物质的量是0.21mol
C.氧化性ClO-<ClO3-
D.ClO3-的生成是由于温度升高引起的
查看答案和解析>>
科目: 来源: 题型:
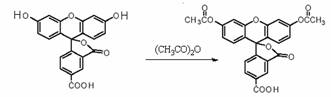
2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质, 5-羧基荧光素与5-羧基二乙酸荧光素在碱性条件下有强烈的绿色荧光,它们广泛应用于荧光分析等。
![]()
下
下列说法不正确的是
A.荧光蛋白遇CuSO4溶液发生盐析
B.5-FAM的分子式为:C21H12O7
C.5-FAM和5-CFDA 各1mol分别与足量NaOH溶液反应,消耗的氢氧化钠物质的量相同
D.荧光蛋白水解可获得多种氨基酸
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是
A .向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至Al3+完全沉淀
Al3++SO42-+Ba2++3OH- = Al(OH)3↓+ BaSO4↓
B.碳酸氢钡溶液中加入过量氢氧化钠溶液:
Ba2++HC03-+OH―=BaC03↓+H20
C.高锰酸钾与乙醇制备Mn3O4纳米粉体,同时生成乙醛:
6MnO4-+13CH3CH2OH→2Mn3O4+13CH3CHO+6OH-+10H2O
D.用惰性电极电解硫酸铜溶液:Cu2++4H2O = Cu+4H++O2↑
查看答案和解析>>
科目: 来源: 题型:
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
A.铈的冶炼步骤为:用稀土串级萃法对矿石进行筛选富集;电解熔融Ce02。
B.Ce02铈溶于氢碘酸的化学方程式可表示为:Ce02+4HI=CeI4+2 H2O
C.用Ce(S04)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.四种稳定的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同位素
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
![]() A.雪碧等碳酸型饮料的PH小于7,晃动后打开瓶盖,PH将变小
A.雪碧等碳酸型饮料的PH小于7,晃动后打开瓶盖,PH将变小
![]() B.晶体在发生物理变化时,也有可能使化学键断裂
B.晶体在发生物理变化时,也有可能使化学键断裂
![]() C.HI、HBr、HCl、HF四种物质的沸点依次降低
C.HI、HBr、HCl、HF四种物质的沸点依次降低
![]() D.周期表中的非金属元素都位于主族
D.周期表中的非金属元素都位于主族
查看答案和解析>>
科目: 来源: 题型:
F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物。已知XeF4与水可发生如下反应:
①6XeF4(s)+12H2O(l)==2XeO3(aq)+4Xe(g)+24HF(aq)+3O2(g) △H=-a KJ/mol
② XeF4(s)+2H2O(l)=Xe(g)+O2(g)+4HF(aq) △H=-b KJ/mol
③3XeF4(s)+6H2O(l)=Xe(g)+2XeO3(aq)+12HF(aq) △H=-c KJ/mol
其中有一半物质的量的XeF4与H2O发生反应②;另一半物质的量的XeF4与H2O发生反应③。下列判断中正确的是
A.XeF2分子中各原子均达到8电子结构
B.a=3b+c
C.XeF4按题给的方式水解,反应中氧化剂和还原剂的物质的量之比为2∶1
D.XeF4按题给的方式水解,每生成4molXe,转移12mol电子
查看答案和解析>>
科目: 来源: 题型:
常温下在下列溶液中,各组离子一定能够大量共存的是
A.在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
C.在c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、ClO -
D.能使碘化钾淀粉试纸变蓝的无色溶液:K+、Fe2+、SO42-、Cl-
查看答案和解析>>
科目: 来源: 题型:
工业上可用下列反应来制取纯硅:
![]() 反应①:Si(粗硅)+3HCl(g)=SiHCl3(l)+H2(g) 反应②:SiHCl3(l)+H2(g) = Si(纯硅)+3HCl(g)
反应①:Si(粗硅)+3HCl(g)=SiHCl3(l)+H2(g) 反应②:SiHCl3(l)+H2(g) = Si(纯硅)+3HCl(g)
假设在每一轮次的投料生产中,硅元素无损失,反应①中HCl的利用率为60%,反应②中H2的利用率为80%。则下一轮次的生产中,需补充投入HCl 和H2的体积比为
A. 4 :1 B. 8:1 C. 2:3 D. 3:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com