
科目: 来源: 题型:
(8分)黄铜矿(CuFeS2)在沸腾炉中与氧气反应(ΔH<0), 生成物冷却后经溶解、除铁、结晶,得到CuSO4?5H2O。实验结果如下:
沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 | |
生 成 物 | 水溶性Cu/% | 90.1 | 91.2 | 93.5 | 92.3 | 89.9 | 84.2 |
酸溶性Cu/% | 92.0 | 93.6 | 97.0 | 97.8 | 98.1 | 98.9 | |
酸溶性Fe/% | 8.5 | 6.7 | 3.4 | 2.7 | 2.3 | 2.8 | |
(1)冷却后的固体中含铜化合物的化学式有 。
(2)除铁时,应将溶液中可能含有的Fe2+离子完全转化为Fe3+离子,转化时最好选用的试剂是 ,然后再加入稍过量的 ,充分反应后过滤。
已知氢氧化物开始沉淀及沉淀完全时的pH:Fe(OH)3(2.7~3.7),Cu(OH)2(5.2~6.4).
(3)实际生产过程的沸腾炉温度适宜控制在 范围最好。控制反应温度的方法是 。
(4)温度高于600℃生成物中水溶性Cu(%)下降的原因是 。
查看答案和解析>>
科目: 来源: 题型:
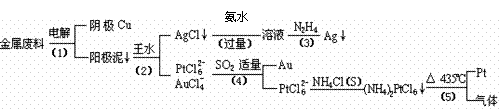
(10分)从含银、锌、金和铂的金属铜废料中提取金、银、铂的一种工艺如下:高考资源网
(王水:浓硝酸与浓盐酸的混合物)高考资源网
 高考资源网
高考资源网
高考资
根据以上工艺回答下列问题:
(1)电解时,以铜金属废料为阳极,纯铜为阴极,CuSO4溶液为电解液,写出阳极电极反应方程式: 。
(2)肼(N2H4)是火箭发射常用的一种液体燃料,其完全燃烧时生成两种无污染的气体。已知部分共价键的键能数据如下表:
化学键 | N-N | O=O | N≡N | O-H | N-H |
键能/kJ?mol-1 | 193 | 499 | 941 | 460 | 393 |
则肼完全燃烧时的热化学方程式为: ;
(3)写出步骤(4)的离子反应方程式: ;
(4)金和浓硝酸反应的化学方程式为:Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O。但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释原因: 。
(5)已知室温下(NH4)2PtCl6的Ksp约为9×10-6。步骤(4)所得溶液中PtCl62-浓度为1×10-4mol?L- 1,则要从1 m3的该溶液中开始析出(NH4)2PtCl6沉淀至少需加入NH4Cl固体的质量为 kg。(设溶液体积的变化忽略不计)
查看答案和解析>>
科目: 来源: 题型:
Mg2+和Al3+的混和溶液中逐滴加入NaOH溶液,形成沉淀的情况出现两种图示。图1为小杨同学绘制,图2是小周根据实验结果绘制,查阅沉淀生成和Al(OH)3溶解的pH情况如表。下列说法正确的是高考资源网

A. 据图计算得n(Mg2+): n(Al3+)=2:1高考资源网
B. 小周实验中,OA段生成两种沉淀高考资源网
C. 图2中OA段表示仅生成Al(OH)3沉淀,AB段仅生成 Mg(OH)2高考资源网
D. 结合表中数据和图2分析,AB段可能发生:Mg2++2AlO2―+4H2O= 2Al(OH)3↓+Mg(OH)2↓
查看答案和解析>>
科目: 来源: 题型:
已知常温时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol?L-1 CH3COOH溶液中逐滴加入0.1 mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误的是高考资源网
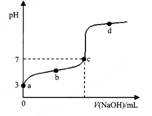 A.a点表示的溶液中c(CH3COO-)略小于10-3 mol?L-1高考资源网
A.a点表示的溶液中c(CH3COO-)略小于10-3 mol?L-1高考资源网
B.b点表示的溶液中c(CH3COO-)>c(Na+)高考资源网
C.c点表示CH3COOH和NaOH恰好反应完全高考资源网
D.b、d点表示的溶液中![]() 均等于K高考
均等于K高考
查看答案和解析>>
科目: 来源: 题型:
锰酸锂离子蓄电池是第二代锂离子动力电池。它的问世使得锂离子动力电池在纯电动汽车与混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:![]() ,下列有关说法错误的是高考资源网
,下列有关说法错误的是高考资源网
A.放电时电池的正极反应式为:Li1-xMnO4+xLi++xe-=LiMnO4高考资源网
B.放电过程中,电极正极材料的质量增加高考资源网
C.充电时电池内部Li+向阴极移动高考资源网
D.充电时电池上标注有“+”的电极应与外接电源负极相连高查看答案和解析>>
科目: 来源: 题型:
下图曲线为某固体饱和溶液浓度随温度变化的情况(该固体从溶液中析出时不带结晶水).下列判断错误的是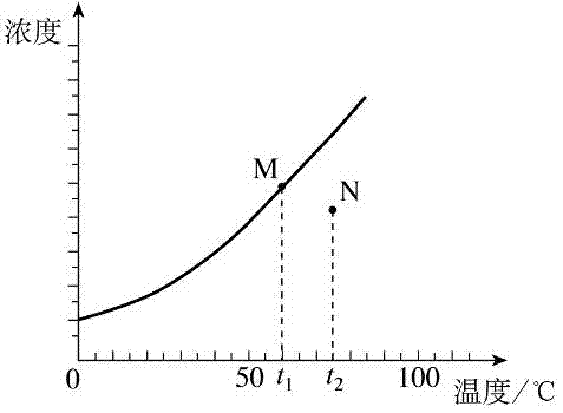 高考
高考
A. 都升温10℃后,M、N点均向右平移高考资源网
B. 加水稀释(假设温度都不变)时,M、N点均垂直向下移动高考资源网
C. 都降温10℃后,M点沿曲线向左下移,N点向左平移至曲线高考资源网
D. 恒温蒸发溶剂至均有晶体析出,则M点不动,N点垂直向上直至曲线相交网
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com