
科目: 来源: 题型:
钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A.2H2O + O2 + 4e → 4OH-
B.Fe 2e → Fe2+
C.2H+ + 2e → H2
D.Fe 3e → Fe3+
查看答案和解析>>
科目: 来源: 题型:
黑火药爆炸时的主要反应是:S + 2KNO3 + 3C → K2S + 3CO2↑ + N2↑,下列说法正确的是
A.上述反应的生成物都是无毒的,所以燃放爆竹时不会污染环境
B.该反应的发生需要点燃或撞击,所以它是一个吸热反应
C.硫磺在黑火药爆炸的反应中既是氧化剂,又是还原剂
D.KNO3有强氧化性,乘坐汽车、火车、飞机时不能随身携带
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.食品添加剂对人体一定是有害的
B.煤的气化和液化是高效、清洁地利用煤炭的重要途径
C.pH小于7.0的雨水通常称为酸雨
D.含磷合成洗涤剂易于被细菌分解,故不会导致水污染
查看答案和解析>>
科目: 来源: 题型:
工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:
2C4H10+5O2![]() 4CH3COOH+2H2O
4CH3COOH+2H2O
现用58吨丁烷为原料制取醋酸,求:
(1)理论上需要标准状况下的空气 m3(设空气中O2、N2的体积分数分别为0.2、0.8),同时生成水 吨。
(2)若生成的醋酸溶解在生成的水中,所得醋酸的质量分数为 %。
(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且![]() ,需补充水y吨,则y与x的关系式为 ;若不补充水,
,需补充水y吨,则y与x的关系式为 ;若不补充水,![]() 则m1+m2= 。
则m1+m2= 。
查看答案和解析>>
科目: 来源: 题型:
白云石化学式为CaCO3?x MgCO3。以它为原料,可制取耐火材料MgO等。称取27.6 g白云石样品,高温加热到质量不再变化,收集到CO2的体积为6.
(1)计算白云石化学式中的X值
(2)该样品高温条件下充分反应后剩余固体的质量?
(3)该样品高温条件下充分反应后剩余固体中MgO的质量?
查看答案和解析>>
科目: 来源: 题型:
某有机物X(C11H9O6Br)分子中有多种官能团,其结构简式为:![]()
(其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如下转化
![]()
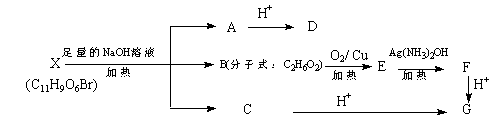
已知向D的水溶液中滴入FeCl3溶液发生显色反应,滴入NaHCO3溶液有无色无味气体产生,且D苯环上的一氯代物有两种。
![]() (1)D中含氧官能团的名称: ;X的结构简式:
(1)D中含氧官能团的名称: ;X的结构简式: ![]()
(2)写出B→E的化学方程式:
(3)D不可能发生的反应有:
A.加成反应 B.消去反应 C.取代反应 D.氧化反应 E.加聚反应
(4)D有多种同分异构体,遇FeCl3溶液发生显色反应,又能发生银镜反应,其中能水解的同分异构体的结构简式为: ,其中不能水解的同分异构体的结构简式为: (各写出一种)
查看答案和解析>>
科目: 来源: 题型:
某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。(图中部分反应条件及产物没有列出)![]()
![]()

(1)写出下列物质的结构简式:
高分子化合物F___________________;六元环状化合物I___________________。
(2)C→D的反应类型为_________________D→E的反应类型为_____________。
(3)写出下列反应的化学方程式:A→B_________________________________________________________
C→可降解塑料_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。”为此,他们设计了如下图所示的装置。
![]()

![]() 请回答下列问题
请回答下列问题
![]() (1) 实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是
(1) 实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是![]() ;装置中B瓶的作用是 。
;装置中B瓶的作用是 。
![]() (2)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是
(2)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是
![]() ;实验发现,通入的O2温度高低对实验现象有较大影响,为便于观察应通入(填“热”或“冷”) 的O2。
;实验发现,通入的O2温度高低对实验现象有较大影响,为便于观察应通入(填“热”或“冷”) 的O2。
![]() (3)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是
(3)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是 ![]() 。
。
(4)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5 mol/L;实验后A中溶液:V=40mL c(H+)=1.0 mol/L。假设反应中HNO3既无挥发也无分解,则
①参加反应的HNO3的物质的量为 mol。
②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中Cu的质量分数还需测定的数据是 。
(5)若已知Cu、Ag合金的质量为m g,且溶解完全。请利用A装置中反应后的溶液进行简单的操作,以确定合金中Cu的质量分数,其实验过程为 。
查看答案和解析>>
科目: 来源: 题型:
设反应CO2(g) + H2(g)![]() CO(g) + H2O(g) 的平衡常数为K,在不同温度下,K 的值如下:
CO(g) + H2O(g) 的平衡常数为K,在不同温度下,K 的值如下:
温度 | 830℃ | 1200℃ |
K | 1 | 2.6 |
(1)从上表可以推断:该反应的逆反应是 (填“吸”、“放”)热反应。
(2)在一体积为10 L的密闭容器中,加入一定量的CO2和H2(g),在830℃时发生上述反应,容器中各物质的浓度变化(mol/L)见下表:
时间/min | CO2 | H2 | CO | H2O |
0 | 0.100 | 0.100 | 0 | 0 |
2 | 0.065 | 0.065 | 0.035 | 0.035 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.050 | 0.050 | 0.050 | 0.050 |
6 | 0.035 | 0.0350 | 0.065 | c4 |
①前2min,用CO2表示的该化学反应的速率是
②表中3min―4min之间反应处于_________状态
③表中第5min时,该反应是否处于化学平衡状态? (填“是”或“否”),此时化学反应速率是ν正 ν逆(填“大于”、“小于”或“等于”),其原因是
④表中5min―6min之间数值发生变化,可能的原因是
a.减少了水蒸气 b.升高温度 c.使用催化剂 d.增大压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com