
科目: 来源: 题型:
反应2A(g)![]() 2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是
2B(g)+C(g)是放热反应,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是
A.升温 B.增大反应器的体积 C.增大c(A) D.降温
查看答案和解析>>
科目: 来源: 题型:
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2在相同温度下发生反应:2SO2+O2![]() 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
A等于p% B大于p% C小于p% D无法判断
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目: 来源: 题型:
已知:4NH3(g)+5O2(g)=4NO(g)+6H2(g). △H=-1025kJ/mol该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
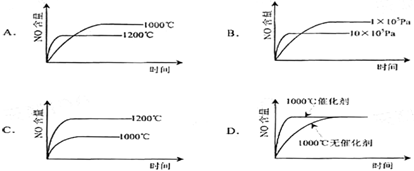
查看答案和解析>>
科目: 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g);△H=+QkJ?mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g);△H=+QkJ?mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.反应至4min时,若HCl的浓度为0.12mol?L-1,则H2的反应速率为0.03mol/(L?min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol?L-1的NaOH恰好反应
查看答案和解析>>
科目: 来源: 题型:
下列各组离子一定能大量共存的是
A.在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+
B.在强碱溶液中:Na+、K+、CO32-、NO3-
C.在pH=12的溶液中:NH4+、Na+、SO42-、Cl-
D.在c(H+)=0.1mol?L-1的溶液中:K+、I-、Cl-、NO3-
查看答案和解析>>
科目: 来源: 题型:
对平衡CO2(g)![]() CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是
CO2(aq);△H= -19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是
A.升温增压 B.降温减压 C.升温减压 D.降温增压
查看答案和解析>>
科目: 来源: 题型:
钢铁发生吸氧腐蚀时,正极上发生的电极反应是
A、2H+ +2e- = H2↑ B、Fe2+ + 2e- = Fe
C、2H2O + O2 + 4e- = 4OH- D、Fe3+ + e- = Fe2+
查看答案和解析>>
科目: 来源: 题型:
在实验室中做下列实验:把物质A、B按一定比例充入一个表面积为300![]() ,容积为2 L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:
,容积为2 L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:
2A(g)+B(g)![]() 2C(g);H=-180 kJ?
2C(g);H=-180 kJ?![]()
 (1)若平均每分钟生成0.5 mol的C,则此反应速率可表示为v(C)=____________;若容器表面向外散热速率平均为400 J?
(1)若平均每分钟生成0.5 mol的C,则此反应速率可表示为v(C)=____________;若容器表面向外散热速率平均为400 J?![]() ?
?![]() ,为了维持恒温t℃,平均每分钟需用加热器提供________kJ的热量;
,为了维持恒温t℃,平均每分钟需用加热器提供________kJ的热量;
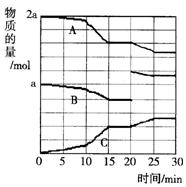
(2)反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断下列说法正确的是_____ ___。
A.10~15 min可能是加入了正催化剂
B.10~15 min可能是降低了温度
C.20 min时可能是缩小了容器体积
D.20 min时可能是增加了B的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com