
科目: 来源: 题型:
![]() -NMR(核磁共振)可用于含碳化合物的结构分析,
-NMR(核磁共振)可用于含碳化合物的结构分析,![]() 表示的是
表示的是
A.核外有13个电子,其中6个能参与成键
B.核内有6个质子,核外有7个电子
C.质量数是13,原子序数是6,核内有7个质子
D.质量数是13,原子序数是6,核内有7个中子
查看答案和解析>>
科目: 来源: 题型:
(7分)主族元素R的最高价氧化物0.112g,溶于水制得100g碱性溶液,其溶质的质量分数为0.148%,R原子核内含有20个中子。通过计算确定R元素在周期表中的位置。(要求写出解题过程)
查看答案和解析>>
科目: 来源: 题型:
5分)市场上出售的“热敷袋”其中的成分主要是铁粉、炭粉、木屑和少量氯化钠、水等。热敷袋用塑料袋密封,使用时从袋中取出轻轻揉搓就会放出热量,用完后袋内有大量铁锈(主要成分Fe2O3)生成,回答下列各问题:
(1)热敷袋放出的热是由于 。
(2)已知有关的电极反应式为负极:Fe-2e-==Fe2+;正极:2H2O+O2+4e-==4OH-,
请写出电极总反应方程式和生成铁锈的化学方程式:
① ;
② ;
③ 。
查看答案和解析>>
科目: 来源: 题型:
(7分)不同元素的气态原子失去最外层的1个电子所需要的能量(设其为E)如下图所示。试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
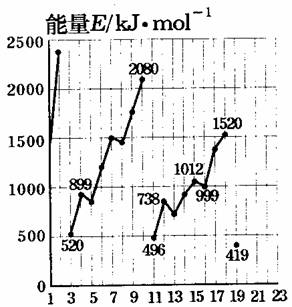
原子序数1至19号元素气态原子失去最外层的1个电子所需能量
(1)同主族内不同元素的E值变化的特点是:______________。各主族中E值的这种变化特点体现了元素性质的______________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系式中正确的是______________。(填写编号,多选倒扣分)
①E(砷)>E(硒) ②E(砷)<E(硒)
③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层的1个电子所需能量E值的范围:
______________<E<______________。
(4)10号元素E值较大的原因是__________________________________。
查看答案和解析>>
科目: 来源: 题型:
(6分)化合物A是一种不稳定的物质,它的分子组成可用OxFy表示,10mLA气体能分解生成15mLO2和10mLF2(同温同压)
(1)A的化学式是__________。
(2)已知A分子中x个氧原子呈…O―O―O…链状排列,则A分子的电子式是______________,…O―O―O…链状排列中中间氧的价态为 。查看答案和解析>>
科目: 来源: 题型:
(7分)(1)下列各组物质①O2和O3 ②H、D和T ③12C和14C④正丁烷(CH3CH2CH2CH3 )和异丁烷[(CH3)2CHCH3] ⑤CH3 CH3、CH3(CH2)3CH3
(请在横线上填写序号)互为同分异构体的是 _,互为同位素的是 ,互为同素异形体的是 ,互为同系物的是 _。
(2)按要求填写下列空白:①NaCl ②KOH ③NH4Cl ④O2 ⑤HCl ⑥He ⑦冰几种物质中,只含有离子键的是________,含有共价键的是________,分子间存在氢键的是_________。
查看答案和解析>>
科目: 来源: 题型:
(10分)某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
实验方案 | 实验现象 |
①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
②向新制的H2S饱和溶液中滴加新制的氯水 | (B)产生气体,可在空气中燃烧,溶液变成浅红色 |
③钠与滴有酚酞试液的冷水反应 | (C)反应不十分强烈,产生的气体可以在空气中燃烧 |
④镁带与2 mol?L-1的盐酸反应 | (D)剧烈反应,产生可燃性气体 |
⑤铝条与2 mol?L-1的盐酸反应 | (E)生成白色胶状沉淀,既而沉淀消失 |
⑥向AlCl3溶液滴加NaOH溶液至过量 | (F)生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:探究同周期元素的金属性和非金属性的递变规律。
(2)实验用品:仪器:① ② ③ ④ 试管夹 ⑤ 镊子 ⑥ 小刀 ⑦ 玻璃片⑧ 砂纸⑨ 烧杯等;
药品:钠、镁带、铝条、2 mol?L-1的盐酸、新制的氯水、饱和的H2S溶液、AlCl3溶液、NaOH溶液等。
(3)实验内容:(填写与实验方案相对应的实验现象)
① ② ③ ④ ⑤ ⑥ (用A-F表示)
写出③的离子方程式 。
(4)实验结论: 。
查看答案和解析>>
科目: 来源: 题型:
化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能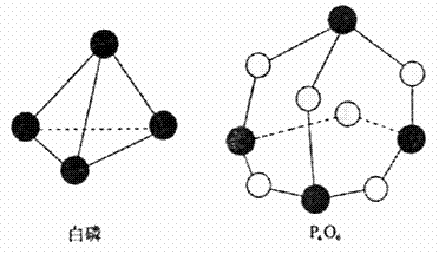 量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P―P:198 P―O:360 O==O:498。则反应P4(白磷)+3O2=P4O6的能量变化为
量。已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P―P:198 P―O:360 O==O:498。则反应P4(白磷)+3O2=P4O6的能量变化为
A.释放1638kJ的能量 B.吸收1638kJ的能量
C.释放126kJ的能量 D.吸收126kJ的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com