
科目: 来源: 题型:
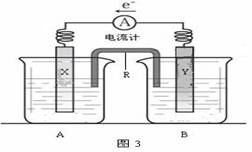
图3是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)== ZnSO4(aq) + Cu(s)。
请回答以下问题:
⑴R的名称是____________,其作用是____________________________________。R中的阳离子移向_______(填A或B)中的溶液。
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的______极,其电极反应式是____________________________。
查看答案和解析>>
科目: 来源: 题型:
向盛有1 mL 0.1 mol/L MgCl2溶液的试管中滴加1~2滴2 mol/L NaOH溶液,观察到有白色沉淀生成,该反应的离子方程式是______________________________。再滴加2滴0.1 mol/L FeCl3溶液,观察到白色沉淀转化为红褐色沉淀,该反应的离子方程式是____________________________________________。由以上现象可以推知,相同条件下Mg(OH)2和Fe(OH)3中溶解度较大的是_________________。
查看答案和解析>>
科目: 来源: 题型:
⑴常温下,0.10 mol/L NH4Cl溶液pH____7(填>、=、<),溶液中各离子浓度由大到小的顺序是______________________________。
⑵相同物质的量浓度的Na2S溶液与NaHS溶液,pH大小: Na2S____NaHS(填>、=、<),两种溶液中微粒种类:Na2S_______NaHS(填>、=、<)。
⑶NaHCO3溶液呈碱性的原因是________________________________(写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是________________________________,将NaHCO3溶液跟Al2(SO4)3溶液混合,现象是___________________________,相关反应的离子方程式是________________________________
查看答案和解析>>
科目: 来源: 题型:
由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式
_______________________
若1 g水蒸气转化成液态水时放热2.444 kJ,则反应H2(g) + 1/2O2(g) == H2O(l)的△H = kJ?![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
已知0.02 mol?L-1CH3COOH溶液和0.01 mol?L-1NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的
A.c (CH3COO-)>c (Na+)
B.c (Na+) + c (H+) =c (
C.c (CH3COOH)>c (CH3COO-)
D.c (CH3COOH)+c (CH3COO-)=0.02 mol?L-1
查看答案和解析>>
科目: 来源: 题型:
某学生设计了一个“黑笔写红字”的趣味实验. 滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上, 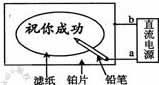 接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此下列叙述正确的是
接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此下列叙述正确的是
A.铅笔芯作阳极,发生还原反应
B.铂片作阴极,发生氧化反应
C.铅笔尖附近有少量的氯气产生
D.红字是H+放电,破坏了水的电离平衡,c(OH-)增大造成
查看答案和解析>>
科目: 来源: 题型:
用某浓度的HCl溶液滴定某浓度的NaOH溶液25.00 mL,滴定曲线如图2所示。则HCl溶液与NaOH溶液的物质的量浓度可能是 (单位:mol?L-1)
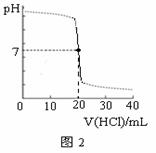
| A | B | C | D |
HCl | 0.12 | 0.10 | 0.10 | 0.08 |
NaOH | 0.10 | 0.12 | 0.08 | 0.10 |
查看答案和解析>>
科目: 来源: 题型:
如右图所示,两个连通容器用活塞分开,左右两室各充入一定量NO和O2,且恰好使两容器内气体密度相同,打开活塞,使NO与O2充分反应,最终容器内混合气体密度比原来
![]()
A .增大 B. 减小 C. 不变 D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com