
科目: 来源: 题型:
用15.8g高锰酸钾氧化密度为1.19g/cm3,质量分数为36.5%的盐酸以制取氯气。反应如下:
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
求:(1)生成Cl2在标况下的体积;
(2)被KMnO4氧化的盐酸的体积;
(3)反应中转移的电子总数。
查看答案和解析>>
科目: 来源: 题型:
(10分)对一定的KClO3加热使其部分分解,然后向反应后的混合物中加入足量的浓硫酸并加热,发生如下反应:KClO3 + 5KCl + 3H2SO4= 3Cl2↑+ 3K2SO4 + 3H2O。假设原KClO3为m mol,第一步反应KClO3分解率为a,两步反应生成的O2与Cl2总物质的量为n mol。
⑴计算当氯元素全部转化为Cl2时的a值及n与m的函数关系式。
⑵讨论在a取不同值时,n与a、m的函数关系式及n的最大值。
查看答案和解析>>
科目: 来源: 题型:
(6分)某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、I―、CO32-,取该溶液进行下述实验:
(1)PH试纸检验,该溶液呈强酸性;
(2)取部分溶液,滴入几滴氯水,再加入少量四氯化碳,振荡后静置,四氯化碳层呈紫红色;
(3)另取部分溶液,逐滴加入NaOH溶液,使溶液由酸性逐渐呈碱性,然后再加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,判断原溶液中肯定存在 离子;
肯定不存在 离子;可能存在 离子。(填化学式)
查看答案和解析>>
科目: 来源: 题型:
(2分)下列有关仪器刻度位置的叙述正确的是
A.容量瓶的体积标线刻在瓶颈上
B.量筒的“0”标线在中间;
C.量筒最下端刻有“0”标线;
D.托盘天平标尺“0”刻度线在标尺的中间。
查看答案和解析>>
科目: 来源: 题型:
(3分)右图为化学教学中常用的喷泉实验装置。其中烧瓶体积为VL,用排空气收集了HCl气体,瓶中的气体对H2的相对密度为17.5。在胶头滴管及烧杯中分别盛有水。将胶头滴管中水挤压入烧瓶,打开止水夹就可引发喷泉,当喷泉停止后,进入烧瓶中水的体积为 。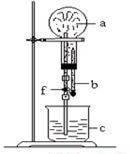
查看答案和解析>>
科目: 来源: 题型:
(12分)室温下,单质A、B、C分别为常见金属、黄绿色气体、无色气体,在合适反应条件下,它们可以按下面框图进行反应,又知E溶液是无色的。
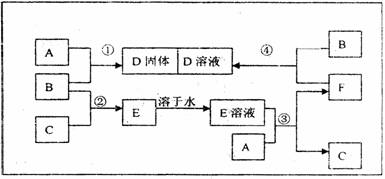
请回答下列问题:
(1)A是 B是 ;(填化学式)
(2)反应①的化学方程式为 ;
(3)反应③的化学方程式为 ;
(4)反应④的化学方程式为 ;
(5)已知D溶液可使淀粉碘化钾试纸变蓝,写出其反应的化学方程式并用双线桥表示电子转移
。
查看答案和解析>>
科目: 来源: 题型:
(10分)漂白粉在生活、工业生产中用途广泛,漂白粉除了具有漂白作用外,还能杀菌消毒。2003年抗“非典”期间,各商场漂白粉及其他漂白产品曾一度脱销。
(1)用Cl2和石灰乳制作漂白粉的反应方程式
其成分是 有效成分是 (填名称)
(2)用Cl2和石灰乳制作漂白粉的目的是 ( )
A.转变为较HclO稳定且易储运的物质 B.转变为更易溶于水的物质
C.提高氯气原利用率 D.增强漂白能力
(3)瓶装漂白粉久置空气中会失效。用化学方程式表示漂白粉在空气中易失效的原因:
①
② 。
查看答案和解析>>
科目: 来源: 题型:
用焰色反应检验K+离子时的操作步骤有:①蘸取待测液,②置于酒精灯火焰上灼烧,③透过蓝色钴玻璃观察,④用稀盐酸洗净铂丝。其中正确的操作顺序为
A.①②③④ B.④①②③ C.①③②④ D.④②①②③
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式相同的一组是:
A.CH3COOH+NaHCO3 = CH3COOH+Na2CO3=;
B.AgNO3+NaCl= AgNO3 + HCl=;
C.Ba(OH)2+H2SO4= BaCl2+H2SO4=;
D.KOH+NH4Cl= NaOH+HCl=;
查看答案和解析>>
科目: 来源: 题型:
有Mg、Al、Fe、Cu四种金属,若两两混合,取26 g混合物与足量稀硫酸反应,产生11.2 L H2(标准状况),此混合物的组合的方式最多有
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com