
科目: 来源: 题型:
(7分)A~I是中学化学中的常见物质,其转化关系如下图所示(已略去部分反应条件):
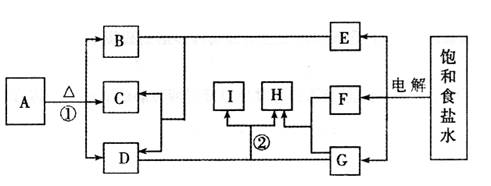
请回答下列问题:
(1)B的名称是 ,F的化学式是 ;
(2)反应①的化学方程式为 ;
(3)反应②的离子方程式为 ;
(4)除上述推断外,你认为A还可以是 (填化学式)
查看答案和解析>>
科目: 来源: 题型:
(7分)氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40℃~50℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+ === Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是 (填“氧化剂”或“还原剂”);
(2)CuH在氯气中燃烧的化学反应方程式为 ;
(3)CuH溶解在稀盐酸中生成的气体是 (填化学式);
(4)如果把CuH溶解在足量的稀硝酸中只生成NO气体,请写出CuH溶解在足量稀硝酸中反应的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
(8分)A、B、C、D、E、F属于短周期主族元素。其中A元素原子是短周期中原子半径最大的原子,B是最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻;F元素原子的核外电子数是C元素原子的2倍。A、B、C三种元素可组成化合物X,C、D可组成化合物Y,C、E可组成化合物Z。
(1)写出下列元素的元素符号:B ,D ,F ;
(2)A~F所形成的简单离子中,与Mg2+具有相同电子层结构的是 。(用离子符号表示);
(3)化合物Z与X的水溶液反应的离子方程式为 ;
(4)化合物Y用途广泛,试列举其中一种用途 。
查看答案和解析>>
科目: 来源: 题型:
(6分)已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物放出或吸收的热量 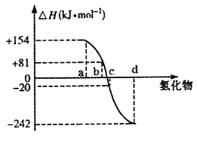 叫该化合物的生成热。右图为氧族元素(钋除外)氢化物a、b、c、d的生成热数据示意图。
叫该化合物的生成热。右图为氧族元素(钋除外)氢化物a、b、c、d的生成热数据示意图。
试回答下列问题:
(1)氧族元素中含18e-的两种氢化物的电子式为
、
;
(2)非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为 ;
(3)硒化氢在热力学标准态下,发生分解反应的热化学反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
碳酸铜和碱式碳酸铜[Cu2(OH)2CO3]均可溶于盐酸转化为氯化铜。在高温下这两种化合物均能分解生成氧化铜。溶解28.4g的上述混合物,消耗1.0mo?L-1盐酸l500mL。灼烧等量的上述混合物,得到的氧化铜质量是
A.15g B.20g C.30g D.35g
查看答案和解析>>
科目: 来源: 题型:
下表是四个反应的有关信息:
序号 | 氧化剂 | 还原剂 | 其它反应物 | 氧化产物 | 还原产物 |
① | Cl2 | FeBr2 |
|
| FeCl3 |
② | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
③ | KClO3 | HCl(浓) |
| Cl2 | Cl2 |
④ | KMnO4 | HCl(浓) |
| Cl2 | MnCl2 |
下列结论正确的是
A.第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较:H2O2>Mn2+>Cl-
D.第③组反应的产物还有KCl和H2O
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、M、N分别代表五种金属。有以下化学反应
①水溶液中:X+Y2 === X2+Y
②Z+2H2O(冷)=== Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M→M2++2e-
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
A.N<M<Y<X<Z B.N<M<X<Y<Z
C.M<N<Y<X<Z D.X<Z<N<M<Y
查看答案和解析>>
科目: 来源: 题型:
据媒体报道:以氢氧燃料电池为动力的公交车即将试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。 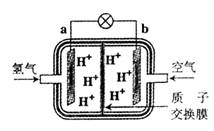 该燃料电池(如图所示)以氢气为燃料,空气为氧化剂,铂作催化剂,用磺酸类物质作溶剂(导电离子是H+)。下列对该燃料电池的描述中正确的是
该燃料电池(如图所示)以氢气为燃料,空气为氧化剂,铂作催化剂,用磺酸类物质作溶剂(导电离子是H+)。下列对该燃料电池的描述中正确的是
A.b为电池的负极
B.负极的反应式为:4H++O2+4e-→2H2O
C.氢离子在电解质溶液中向b极移动
D.总的化学反应可表示为:2H2+O2![]() 2H2O
2H2O
查看答案和解析>>
科目: 来源: 题型:
下列关于铜电极的叙述,不正确的是
A.电池反应为2Ag++Cu=2Ag+Cu2+的原电池中,铜作负极
B.电解法精炼粗铜时,精铜作阴极
C.铁的吸氧腐蚀的负极反应为2H2O+O2+4e- →4OH-
D.在镀件上镀铜时,铜作阳极
查看答案和解析>>
科目: 来源: 题型:
目前,人类已经发现的非金属元素除稀有气体元素外有16种,下列对这16种非金属元素的判断不正确的是
①都是主族元素,原子的最外层电子数都大于3
②单质在反应中都只能作氧化剂
③对应的含氧酸都是强酸
④氢化物常温下都是气态,所以又叫气态氢化物
⑤气态氧化物与水反应都不会再生成气体
A.全部 B.只有①② C.只有①②③④ D.只有①②④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com