
科目: 来源: 题型:
(7分) 化合物A、B和C互为同分异构体。它们的元素分析数据为:碳 92.3%, 氢 7.7%。1 mol A在氧气中充分燃烧产生179.2 L二氧化碳(标准状况)。A是芳香化合物,分子中所有的原子共平面;B是具有两个支链的链状化合物,分子中只有两种不同化学环境的氢原子,偶极矩等于零;C是烷烃,分子中碳原子的化学环境完全相同。
9-1 写出A、B和C的分子式。
9-2 画出A、B和C的结构简式。
查看答案和解析>>
科目: 来源: 题型:
(9分) 由烷基镁热分解制得镁的氢化物。实验测定,该氢化物中氢的质量分数为7.6%,氢的密度为0.101 g cm3,镁和氢的核间距为194.8 pm。已知氢原子的共价半径为37pm,Mg2+ 的离子半径为72 pm。
8-1 写出该氢化物中氢的存在形式,并简述理由。
8-2 将上述氢化物与金属镍在一定条件下用球磨机研磨,可制得化学式为Mg2NiH4的化合物。X-射线衍射分析表明,该化合物的立方晶胞的面心和顶点均被镍原子占据,所有镁原子的配位数都相等。推断镁原子在Mg2NiH4晶胞中的位置(写出推理过程)。
8-3 实验测定,上述Mg2NiH4晶体的晶胞参数为646.5 pm,计算该晶体中镁和镍的核间距。已知镁和镍的原子半径分别为159.9 pm和124.6 pm。
8-4 若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,计算Mg2NiH4的储氢能力(假定氢可全部放出;液氢的密度为0.0708 g cm3)。
查看答案和解析>>
科目: 来源: 题型:
(14分) AX4四面体 (A为中心原子,如硅、锗;X为配位原子,如氧、硫) 在无机化合物中很常见。四面体T1按下图所示方式相连可形成一系列“超四面体”(T2、T3???):
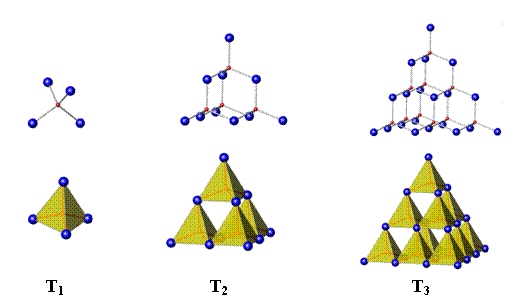
7-1上图中T1、T2和T3的化学式分别为AX4、A4X10和A10X20,推出超四面体T4的化学式。
7-2 分别指出超四面体T3、T4中各有几种环境不同的X原子,每种X原子各连接几个A原子?在上述两种超四面体中每种X原子的数目各是多少?
7-3若分别以T1、T2、T3、T4为结构单元共顶点相连(顶点X原子只连接两个A原子),形成无限三维结构,分别写出所得三维骨架的化学式。
7-4 欲使上述T3超四面体连接所得三维骨架的化学式所带电荷分别为+4、0和 -4,A选Zn2+、In3+或Ge4+,X取S2-,给出带三种不同电荷的骨架的化学式(各给出一种,结构单元中的离子数成简单整数比)。
查看答案和解析>>
科目: 来源: 题型:
(11分) 在900oC的空气中合成出一种含镧、钙和锰 (摩尔比2 : 2 : 1) 的复合氧化物,其中锰可能以 +2、+3、+4 或者混合价态存在。为确定该复合氧化物的化学式,进行如下分析:
6-1 准确移取25.00 mL 0.05301 mol L1的草酸钠水溶液,放入锥形瓶中,加入25 mL蒸馏水和5 mL 6 mol L1的HNO3溶液,微热至60~70oC,用KMnO4溶液滴定,消耗27.75 mL。写出滴定过程发生的反应的方程式;计算KMnO4溶液的浓度。
6-2 准确称取0.4460 g复合氧化物样品,放入锥形瓶中,加25.00 mL上述草酸钠溶液和30 mL 6 mol L1 的HNO3溶液,在60~70oC下充分摇动,约半小时后得到无色透明溶液。用上述KMnO4溶液滴定,消耗10.02 mL。根据实验结果推算复合氧化物中锰的价态,给出该复合氧化物的化学式,写出样品溶解过程的反应方程式。已知La的原子量为138.9。
查看答案和解析>>
科目: 来源: 题型:
(10分) (CN)2被称为拟卤素,它的阴离子CN- 作为配体形成的配合物有重要用途。
4-1 HgCl2 和Hg(CN)2反应可制得 (CN)2, 写出反应方程式。
4-2 画出CN-、(CN)2的路易斯结构式。
4-3 写出(CN)2 (g) 在O2 (g) 中燃烧的反应方程式。
4-4 298 K下,(CN)2 (g) 的标准摩尔燃烧热为 1095 kJ mol1,C2H2 (g) 的标准摩尔燃烧热为 1300 kJ mol1,C2H2 (g) 的标准摩尔生成焓为227 kJ mol1,H2O (l) 的标准摩尔生成焓为 -286 kJ mol1,计算 (CN)2 (g) 的标准摩尔生成焓。
4-5 (CN)2在300~500 oC形成具有一维双链结构的聚合物,画出该聚合物的结构。
4-6 电镀厂向含氰化物的电镀废液中加入漂白粉以消除有毒的CN-,写出化学方程式(漂白粉用ClO表示)。
查看答案和解析>>
科目: 来源: 题型:
(5分) 化合物X是产量大、应用广的二元化合物,大量用作漂白剂、饮水处理剂、消毒剂等。年产量达300万吨的氯酸钠是生产X的原料,92%用于生产X―在酸性水溶液中用盐酸、二氧化硫或草酸还原。此外,将亚氯酸钠固体装柱,通入用空气稀释的氯气氧化,也可生产X。X有极性和顺磁性,不形成二聚体,在碱性溶液里可发生歧化反应。
2-1 写出X的分子式和共轭π键(![]() )。
)。
2-2 分别写出上述用草酸还原和用氯气氧化生产X的反应方程式。
2-3 写出上述X歧化反应的化学方程式。
查看答案和解析>>
科目: 来源: 题型:
X和Y在周期表中相邻。CaCO3与X的单质高温反应,生成化合物B和一种气态氧化物;B与Y的单质反应生成化合物C和X的单质;B水解生成D;C水解生成E,E水解生成尿素。确定B、C、D、E、X和Y。
查看答案和解析>>
科目: 来源: 题型:
取质量相等的2份PbSO4 (难溶物)粉末,分别加入HNO3 ( 3 mol L1) 和HClO4 ( 3 mol L1),充分混合,PbSO4在HNO3 能全溶,而在HClO4中不能全溶。简要解释PbSO4在HNO3中溶解的原因。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com