
科目: 来源: 题型:
今年是勒沙特列(Le Chatelier1850-1936)诞生150周年。请用勒沙特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。(6分)
查看答案和解析>>
科目: 来源: 题型:
1999年是人造元素丰收年,一年间得到第114、116和118号三个新元素。按已知的原子结构规律,118号元素应是第 周期第 族元素,它的单质在常温常压下最可能呈现的状态是 (气、液、固选一填入)态。近日传闻俄国合成了第166号元素,若已知原子结构规律不变,该元素应是第 周期第 族元素。(5分)
查看答案和解析>>
科目: 来源: 题型:
动物之间的信息传递除了声音、光电信号外,在低等动物中,如昆虫,还能分泌化学物质作为种群个体之间的通讯工具,这就是所谓“化学通讯”。棉铃象(一种象鼻虫)的性引诱剂就是这类化学物质。它是混合物,含有单环萜烯醇E和萜烯醛F和H。人工合成棉铃象性引诱剂是杀灭这种棉花害虫的绿色农药。其合成路线如下:

问题:分别写出上面以A、B、C、D、E、G、H为代号的各化合物的结构简式。
查看答案和解析>>
科目: 来源: 题型:
一、早在十六世纪,人们就将古柯叶的提取液用于抗疲劳。1826年Wöhler揭示了其活性成分是可卡因(一种毒品)A(C17H21NO4)。它虽然是很有效的局部麻醉药,但毒性大,易成瘾。A用氢氧化钠水溶液水解,中和后得甲醇,苯甲酸和芽子碱B(C9H15NO3)。B用三氧化铬氧化得C(C9H13NO3),C加热生成含有羰基的化合物D(C8H13NO)并放出一种气体。D在活性镍催化下氢化得到醇E( 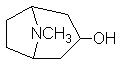 或表示为
或表示为 )
)
二、后来有人通过Mannich反应,以CH3NH2、3-氧代戊二酸与F为反应物,一步反应就合成了D.
提示:(1) b-酮酸在加热时可以脱羧(CO2)生成酮,例如:
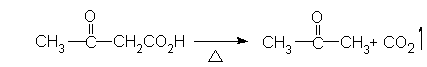
(2) Mannich反应是含有a活泼氢的有机物与胺和甲醛发生三分子之间的缩合反应,放出水分子,该反应可以简单地看作a活泼氢被反应过程中生成的胺烃基取代,例如:
 |
回答下列问题:
1、写出A、B、C、D的结构简式。
2、写出F的结构式。
查看答案和解析>>
科目: 来源: 题型:
在NH4Cl水溶液中用空气氧化碳酸钴(II)可以得到具有光泽的红色氯化物A(NH3:Co:Cl为4:1:1)。将A的固体在0℃下加入用HCl气体饱和的无水乙醇中,在室温下有气体迅速释放,将其振摇至不再有气体发生,得到蓝灰色固体B,B是一种混合物。将B过滤,用乙醇洗涤,然后用少量冷水洗涤, 所得主要产物再经一系列提纯步骤产生紫色晶体C (化学式: CoCl3?4NH3?0.5H2O)。当C在浓盐酸中加热时, 可以分离出一种绿色化合物D, 经分析为CoCl3?4NH3?HCl?H2O。D可溶于冷水,加浓盐酸就沉淀出来。
提示:
① 已知[CoCl2(en)2]+可被拆分的异构体形式是紫色的;并且在溶液中存在如下平衡:
紫色-[CoCl2(en)2]Cl ![]() 绿色-[CoCl2(en)2]Cl?HCl?2H2O
绿色-[CoCl2(en)2]Cl?HCl?2H2O
注:en = H2NCH2CH2NH2
② 在-12℃的低温下,用HCl气体饱和了的盐酸处理如下图所示的双核配合物![]() ,同样能得到C。
,同样能得到C。
回答下列问题:
(1) A~D分别代表何种化合物?请分别画出C与D中配离子的立体结构。
(2) 写出并配平所有的化学方程式。
(3) 试根据C与D中配离子的立体结构判断它们的极性,并简要说明理由。
(4) 用少量冷水洗涤B目的何在?浓盐酸在绿色化合物D形成中起什么作用?
(5) C与D之间的转化属于一种什么类型的反应?
(6) 由题给条件和提示说明你所推测的化学反应发生的依据。查看答案和解析>>
科目: 来源: 题型:
东晋葛洪所著《抱朴子》中记载有“以曾青涂铁,铁赤色如铜”。“曾青”即硫酸铜。这是人类有关金属置换反应的最早的明确记载。铁置换铜的反应节能、无污染,但因所得的镀层疏松、不坚固,通常只用于铜的回收,不用作铁器镀铜。能否把铁置换铜的反应开发成镀铜工艺呢?
从化学手册上查到如下数据:
电极电势:
Fe2++2e == Fe fy == 0.440V;Fe3++e == Fe2+ fy == 0.771V;
Cu2++2e == Cu fy == 0.342V; Cu2++e == Cu+ fy == 0.160V
平衡常数: Kwy = 1.0´10-14; Kspy (CuOH)=1.0´10-14;
Kspy [Cu(OH)2]=2.6´10-19; Kspy [Fe(OH)2]=8.0´10-16;
Kspy [Fe(OH)3]=4.0´10-38;
回答如下问题:
1. 造成镀层疏松的原因之一可能是夹杂固体杂质。为证实这一设想,设计了如下实验:向硫酸铜溶液加入表面光洁的纯铁块。请写出四种可能被夹杂的固体杂质的生成反应方程式(不必写反应条件)。
2. 设镀层夹杂物为CuOH(固),实验镀槽的pH=4,CuSO4的浓度为0.040mol/L,温度为298K,请通过电化学计算说明在该实验条件下CuOH能否生成。
3. 提出三种以上抑制副反应发生的(化学的)技术途径,不必考虑实施细节,说明理由。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com