
科目: 来源: 题型:阅读理解
(12分)白色固态有机酸A含碳、氢和氧元素。为了得到摩尔质量的估值,将10.0g该有机酸溶于水,加入碎冰,激烈摇荡,结果温度降至-2.5℃后迅速除去冰,测得溶液的质量为76.1g,pH值为1.4。由手册中查到,水的摩尔冰点下降常数为1.86kg?K?mol-1。然后,对该酸的准确摩尔质量作了精确测定。0.120g该酸用0.100mol/L的氢氧化钠溶液滴定,以酚酞为指标剂,当指示剂变色时,用去氢氧化钠溶液23.4mL。
5-1 得出该酸(A)的摩尔质量和结构。
液体B溶于水可以达到10%,该溶液的pH值约为4。B不易氧化,但能发生碘仿反应,产物经酸化,氧化成A。0.10gB消耗1.5g碘单质。当B和钠反应,放出氢气,生成一种金属有机化合物X,X阴离子的摩尔质量约为98g/mol。
5-2 写出碘仿反应的化学方程式及上述B与钠的反应,其中的有机物应采用结构式。
化合物C的水溶液的导电性和纯水相差无几。C碱性水解生成氨。0.120g C用热的氢氧化钠稀溶液处理,将生成的气体导入50.0cm3浓度为0.100mol/dm3的盐酸中;剩余的酸用0.100mol/dm3氢氧化钠溶液滴定,消耗10.0cm3。C酸性水解生成二氧化碳。由冰点下降得知C的摩尔质量估值在40~70g/mol之间。
5-3 写出C的结构。写出它的碱性水解及酸性水解的离子方程式。
令C在强碱催化剂存在下与酸A的乙酯反应,生成乙醇和化合物D。D的组成为37.5%(质量分数,下同)C、3.1% H和21.9% N,其余是氧。该化合物是一种酸。
5-4 写出D的结构。其酸性氢原子在何处?请在结构式中用*标出。
查看答案和解析>>
科目: 来源: 题型:
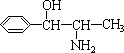 (10分)目前,包括我国在内的许多国家都已经暂停销售和使用含苯丙醇胺的药品制剂。苯丙醇胺的英文名称是Phenylpropanolamine,
(10分)目前,包括我国在内的许多国家都已经暂停销售和使用含苯丙醇胺的药品制剂。苯丙醇胺的英文名称是Phenylpropanolamine,
缩写为PPA,化学结构如右图所示:
4-1 系统命名法命名苯丙醇胺:
4-2 右图上用*标出苯丙醇胺中的手性碳原子,并确定光学异构体数目。
4-3 苯丙醇胺容易和盐酸成盐,生成盐酸苯丙醇胺,而被广泛入药。写出盐酸苯丙醇胺的结构简式
4-4 以常见有机物A为原料,与硝基乙烷作用,所得产物经还原可以很方便地得到苯丙醇胺。合成路线如下:
A+CH3CH2NO2![]() B
B![]() 苯丙醇胺
苯丙醇胺
写出A、B的结构简式。
查看答案和解析>>
科目: 来源: 题型:
(8分)实验表明,乙烯在很低的温度下能凝结成分子晶体,经X-射线分析鉴定,晶胞参数为:a=487pm,b= 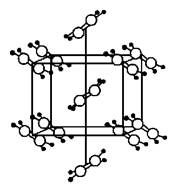 646pm,c=415pm,晶体结构如右图所示。
646pm,c=415pm,晶体结构如右图所示。
3-1 该晶体的晶胞类型是 ;
3-2 晶体的理论密度是 g?cm-3;
3-3 设C原子形成的双键中心对称地通过原点,离原点最近的C原子的分数坐标为(0.11,0.06,0.00),试计算C=C共价键长是 pm。
查看答案和解析>>
科目: 来源: 题型:
(9分)将NH4Cl溶液用盐酸调制成pH = 4的溶液,然后进行电解,发现制成了一种常见的二元化合物A,用空气把气体产物带出电解槽即得到较为纯净的A。A是一种挥发性的易爆炸的浓稠液体,沸点只有700C,其结构与NH3相似。
2-1 试确定A,写出生成A的离子方程式。
2-2 比较A和NH3的极性大小。
2-3 将A与NaClO2按物质的量之比1∶6混合,可得到一种绿色环保的消毒剂B以及能使湿润的红色石蕊试纸变蓝的气体C。A的消毒效果是同质量的Cl2的2.63倍。试写出其反应的离子方程式。
2-4 已知A中两元素的电负性相同。试设计一个试验确定A中哪一种元素带部分正电荷,哪一种元素带部分负电荷?简述其实验步骤。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(18分)下列八个步骤是用来分析一种含铅锡的合金中铅和锡的个别含量
(1)称量0.4062g的合金,放在烧杯中,用11mol?L-1的HCl和16mol?L-1的HNO3溶液溶解样品。在此过程中铅和锡分别被氧化成Pb(II)、Sn(VI)。
(2)再加热5分钟,以赶走氮和氯的氧化物后,使溶液冷却;此时会有一些锡化合物和一种铅化合物沉淀出。
(3)加入25.00mL 0.2000mol?L-1的Na2H2EDTA(可用H2Y2-表示)溶液后,沉淀会溶解成一透明无色的溶液。
(4)上述溶液全部移入250.0mL的量瓶中,并用蒸馏水稀释到量瓶的刻度上。
(5)拿出25.00mL,加入30%的Hexamine(如下图)溶液15mL、H2O及两滴的类苯酚橙(以XO代表)(如下图)当指示剂,此溶液的pH值为6。
(6)再用标准0.009970mol?L-1的硝酸铅Pb(NO3)2 溶液滴定从第(5)步骤中的黄色透明的溶液,直至颜色刚好由黄色变到红色,此实验值为24.05mL。
(7)取2.0g的固体NaF加入滴定瓶中,此时溶液会变回黄色。
(8)再用0.009970mol?L-1的硝酸铅滴定到颜色变红,此实验值为15.00mL。
Hexamine和类苯酚橙(XO)的结构式如下:

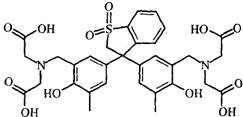
Hexamine 类苯酚橙(XO)
Hexamine的pKb =9.5。类苯酚橙(XO)在pH小于4时是红色,pH大于5时是黄色
回答下列问题
10-1 在步骤(2)中铅的沉淀物是什么?写出其化学式。
10-2 写出步骤(3)中沉淀消失的离子反应方程式(必须平衡)?记得此溶液的pH值为6。
10-3 步骤(5)中为何加入Hexamine?
10-4 加入类苯酚橙(XO)的目的为何?
10-5 写出步骤(6)中,(i)在滴定过程中,以及(ii)滴定终点造成颜色变化时的平衡离子反应方程式。
10-6 步骤(7)中,加入NaF的目的为何?
10-7 写出步骤(7)中的平衡离子方程式。
10-8 用平衡的离子方程式来说明为什么步骤(7)中的颜色会由红变为黄?用XO代表类苯酚橙。
10-9 计算此合金中Pb的重量百分比,再另外计算此合金中Sn的重量百分比。
查看答案和解析>>
科目: 来源: 题型:
(7分)配合物A是临床批准使用的抗癌配合物之一,它有某些不同于顺铂和碳铂的特性,它是由四氯合铂酸钾与B的光学异构体作用,然后与草酸铵反应制得,B在其同分异构体中是最稳定得环状化合物,它的两个官能团处于相邻的位置;A的元素分析实测值为:C:24.64,H:3.51,N:7.05,Pt:49.30,(原子量:C 12.00 H 1.01 N 14.01 O 16.00 Pt 195.08)
9-1 写出Pt(II)离子的电子结构,说明配合物A有无磁性。
9-2 写出B的平面结构式并命名
9-3 写出配合物A的分子式及结构式
查看答案和解析>>
科目: 来源: 题型:
(6分)氰氨化钙(CaCN2)是一种多用途的有机肥料,它很容易用廉价的普通化学品如CaCO3来生产,CaCO3热分解产生白色固体XA和无色气体XB,后者不支持燃烧。用碳还原XA生产灰色固体XC和气体XD,XC和XD能进一步氧化,XC与氮反应,最终生成CaCN2。
8-1 如何合成氰氨化钙,完成下列反应:
(1)CaCO3 ![]() XA+XB
XA+XB
(2)XA+3C![]() XC+XD
XC+XD
(3)XC+N2![]() CaCN2+C
CaCN2+C
8-2 CaCN2水解产生什么气体,写出水解反应方程式
8-3 在固体化学中,CN22-离子呈现异构化,两种异构离子的酸都是已知的(至少在气态),画出这两种异构化酸的结构式,指出异构化平衡更倾向哪一侧。
查看答案和解析>>
科目: 来源: 题型:
 (11分)据Science杂志报道,大气中存在一种潜在的温室气体――SF5-CF3,虽然其数量有限,仅达0.1ppt(见右图),但是它是已知气体中吸热最高的气体。虽然来源未知,但科学家认为它很可能是用作高压电绝缘材料的SF6和含氟高分子反应的产物。
(11分)据Science杂志报道,大气中存在一种潜在的温室气体――SF5-CF3,虽然其数量有限,仅达0.1ppt(见右图),但是它是已知气体中吸热最高的气体。虽然来源未知,但科学家认为它很可能是用作高压电绝缘材料的SF6和含氟高分子反应的产物。
回答下列问题:
7-1 ppt和ppm一样,都是表示微量物质的符号,全名分别是part per trillion和part per million,ppt在环境领域表示万亿分之一,则1 ppm =_______ ppt。
7-2 下列微粒中中心原子杂化类型与高压绝缘材料SF6中S原子杂化类型相似的是 。
A.SiF62- B.PCl3 C.BrF5 D.S2Cl2
7-3 重要含氟高分子之一是![]() CF2-CF2
CF2-CF2![]() ,有“塑料之王”的美名。其名称是________,由_________(结构简式)聚合而成。
,有“塑料之王”的美名。其名称是________,由_________(结构简式)聚合而成。
7-4 画出SF5-CF3的结构式,并写出SF6与 ![]() CF2-CF2
CF2-CF2![]() 反应的方程式。
反应的方程式。
7-5 SF5-CF3中的-CF3是很强的吸电子基团,一般烃基都是给电子基团。试比较下列物质的酸性:H2CO3,C6H5OH,CF3COOH,CH3COOH
7-6 将右图的标题译成中文(化合物用化学式代替)。
查看答案和解析>>
科目: 来源: 题型:
(6分)阿斯巴甜是一种口味好、安全性高的强力甜味,用APM表示。甜度是蔗糖的180~200倍,已广泛应用于食品、饮料及制药行业。鉴于传统的多锅法生产工艺的不合理性,下面的方法研究了上述反应一锅化的可能性,总收率达到了63.6%左右。
HCOOH+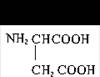 +2
+2 →A+4CH3COOH
→A+4CH3COOH
A+C6H5-CH2-![]() COOH→B(α异构体,主要产物)+C(β异构体)
COOH→B(α异构体,主要产物)+C(β异构体)
B+HCl(aq)+CH3OH→D+F
D+NH3→E(APM)+NH4Cl (以上反应都已配平)
请分别画出A、B、C、D、E、F的结构简式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com