
科目: 来源: 题型:
设NA表示阿伏伽德罗常数的值,下列说法正确的是
A. 0.1molF-中含有的电子数为9NA
B. 1L0.5mol.l-1的CaCl2溶液中所含有的Cl-数为0.5NA
C. 常温常压下,32g氧气中所含的质子数为16NA
D. 标准状况下,11.2L的CH4中含有的氢原子数为NA
查看答案和解析>>
科目: 来源: 题型:
有一白色固体可能是由Al2(SO4)3、AgNO3、BaCl2、NH4Cl、KOH中的两种或三种组成,为确定该白色固体的组成,进行下列实验:取白色固体少许,加入蒸馏水充分振荡得无色溶液;逐滴加入稀HNO3有白色沉淀生成。试回答:
(1) 此白色固体中至少存在哪几种物质?请写出全部可能。
(2) 若要证明固体的组成,还需要做的实验是
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,RO3 n-和 I- 发生的离子方程式如下:
RO3 n-+ 6I- + 6H+ == R- + 3I2 + 3H2O
(1) RO3 n-中R元素的化合价是_____________
(2) R元素的原子最外层电子数是________。
查看答案和解析>>
科目: 来源: 题型:
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 ;
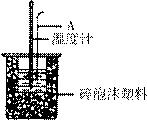 (2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃)。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=________________;(结果保留一位小数)
(4) (填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是 。
查看答案和解析>>
科目: 来源: 题型:
(1)用18mol/L硫酸配制1.0mol/L硫酸100ml,若实验室仪器有:
A:100ml量筒 B:托盘天平C:玻璃棒D;50ml 容量瓶E:10ml量筒F:胶头滴管G:50ml烧杯H: 100ml容量瓶
实验时应选取的仪器先后顺序是(填入编号,下同)
(2)在下列操作中正确的是 使所配溶液浓度偏高的是
A.使用容量瓶前检查它是否漏液
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.配制溶液时,如果试样是固体氢氧化钠,把称好的试样用纸条小心倒入容量瓶中,缓缓加入蒸馏水到接近刻度线2-3cm处,用滴管滴加蒸馏水至刻度线
D.配制溶液时,如果试样是液体如浓硫酸,用量筒量取浓硫酸缓缓地沿玻璃棒倒入盛有蒸馏水的小烧杯中,并不断搅拌,冷却后转移到容量瓶中,并洗涤烧杯2-3次,洗液也移入容量瓶中。
E:盖好瓶塞,用食指顶住瓶塞,用另一只手的手指拖住瓶底,把容量瓶倒转和摇动多次。
F.若定容时加水过量,用吸管吸出。
G.向容量瓶中移液时有少量液体流出
H.定容时仰视标线
I.定容摇匀后液面下降又加水
查看答案和解析>>
科目: 来源: 题型:
肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol
下列表示肼跟N2O4反应的热化学方程式,正确的是
A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol
B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol
C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol
D.N2H4(g)+![]() N2O4(g)=
N2O4(g)=![]() N2(g)+2H2O(g);△H=-1076.7kJ/mol
N2(g)+2H2O(g);△H=-1076.7kJ/mol
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.在101 k Pa时,1 mol C与适量![]() 反应生成1mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ/mol
反应生成1mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ/mol
B.在10l k Pa时,l mol![]() 完全燃烧生成液态水,放出285.8 kJ热量,
完全燃烧生成液态水,放出285.8 kJ热量,![]() 燃烧热为 ―285.8KJ/mol
燃烧热为 ―285.8KJ/mol
C.鉴定HCL和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度
D.在稀溶液中:![]() ,若将含 0.5mol
,若将含 0.5mol![]() 的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ
的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ
查看答案和解析>>
科目: 来源: 题型:
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每摩尔CuSO4能氧化P的物质的量为
A.1/5 mol B.2/5 mol
C.3/5mol D.11/5 mol
查看答案和解析>>
科目: 来源: 题型:
在KClO3+6HCl=KCl+3Cl2+3H2O反应中,当生成0.5molCl2时,氧化产物和还原产物的物质的量之比为
A.6:1 B.5:1
C.1:3 D.1:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com