
科目: 来源: 题型:
下列实验中所选用的仪器合理的是
A 用200ml量筒量取5.2ml稀硫酸
B 用250ml容量瓶配制250ml0.2mol/L的氢氧化钠溶液
C 用托盘天平称量11.7克氯化钠晶体
D 用碱式滴定管量取25.1ml溴水
查看答案和解析>>
科目: 来源: 题型:
下列实验操作正确的是
A. 将氢氧化钠固体放在滤纸上称量
B. 用10ml量筒量取8.58ml蒸馏水
C. 制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D. 配制氯化铁溶液时,将一定量氯化铁溶解在较浓的盐酸中,再用水稀释到所需浓度。
查看答案和解析>>
科目: 来源: 题型:
⑴配位化学创始人维尔纳发现,将等物质的量的CoCl3?6NH3(黄色)、CoCl3?5NH3(紫红色)、CoCl3?4NH3(绿色)和CoCl3?4NH3(紫色)四种化合物溶于水,加入足量硝酸银溶液,立即产生氯化银沉淀的量分别为3mol、2mol、1mol和1mol。
①请根据实验事实用配合物的形式写出它们的化学式。
CoCl3?6NH3 CoCl3?5NH3
CoCl3?4NH3(绿色和紫色):
②后两种物质组成相同而颜色不同的原因是
③上述配合物中,中心离子的配位数都是
⑵向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(KSCN)3是配合物,Fe3+与SCN―不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①Fe3+与SCN―反应时,Fe3+提供 、SCN―提供 ,二者通过配位键结合。
②所得Fe3+与SCN―的配合物中,主要是Fe3+与SCN―以个数比1∶1配合所得离子显血红色。含该离子的配合物的化学式是 。
③若 Fe3+与SCN―以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为 。
④已知SCN―离子中所有原子均满足最外层8电子结构,一个电子是由S原子所得,则SCN―的电子式是 。
查看答案和解析>>
科目: 来源: 题型:
某化工厂制备氯化铜时,是密闭容器中将浓盐酸用水蒸汽加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌,使之溶解,
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;
pH≥4.4时,Cu2+以Cu(OH)2的形式开始沉淀; pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;
pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。
请你仔细阅读以上信息,并回答下列问题:
⑴写出粗制氧化铜粉与浓盐酸反应的化学方程式 。
⑵工业上为除去溶液中的Fe2+,常使用NaClO,当向溶液中加入NaClO,其反应的离子方程式为 。
⑶若此溶液只含Fe3+时,要调整pH在3~4之间,此时最好向溶液中加入 。
⑷25℃时,已知溶液中c(Cu2+)与溶液pH的关系为lg c(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1 mol/L,则溶液pH为___________,此时溶液中的铁离子能否沉淀完全_________(填“能”或“否”),Cu2+是否开始出现沉淀 (填“能”或“否”)。
⑸还需什么操作才能得到CuCl2溶液? 。
查看答案和解析>>
科目: 来源: 题型:
硫酸工业、硝酸工业和合成氨工业是重要的化学工业。
⑴在①硫酸工业②合成氨工业③硝酸工业三大工业中,在生产过程中有化学平衡存在的工业是 ,采用循环操作的是 。(填序号)
⑵过磷酸钙是一种常见的化肥,其有效成份是磷酸二氢钙,则工业上用磷酸钙制取过磷酸钙的化学方程式为 。
⑶合成氨生产中,根据化学平衡原理来确定的条件或措施有 (填写序号)。
A.氮气的制取 B.使用铁触媒作催化剂
C.使用400~500℃的温度 D.及时分离生成的NH3
E.合成氨在高压下进行 F.制水煤气除去CO2
⑷工业上用接触法制硫酸,最后的产品是98%硫酸或20%发烟硫酸(含SO3质量分数为20%的硫酸),若98%硫酸表示为SO3•aH2O,20%发烟硫酸表示为SO3•bH2O,则a,b分别为:a=_________,b=___________。
查看答案和解析>>
科目: 来源: 题型:
三氯化氮是液氯等生产过程中能引起爆炸的一种化合物。由原盐、生产用水中含有的氮氢化合物―――氨随盐水进入电解槽它在电解过程中,与电解产物氯气反应或者是用水洗涤氯气而生成。由于它易分解并释放出大量气体而易发生爆炸事故。在液氯生产过程中,当NCl3质量分数(指NCl3的质量占氯气和NCl3的总质量的百分比)超过5%时即有爆炸的危险。
⑴在氯化铵遇到Cl2时,当PH值<5时,生成三氯化氮的化学方程式: 。
⑵NCl3爆炸时生成N2和C12。已知24.1g NCl3发生上述反应时放出的热量为91.2KJ,则标准状况下2.24LCl2生成时能放出热量 KJ。
⑶某氯碱厂为测氯气中三氯化氮的含量,将样品先用内盛15.0 mL盐酸试剂的吸收管吸收NCl3(NCl3+HCl→NH4Cl+C12,未配平),然后用内盛400 mL 30.0%(ρ=1.22g/cm3)工业氢氧化钠吸收瓶吸收氯气,碱吸收瓶吸收后质量增加77.1g。三氯化氮吸收管内的氯化铵经仪器测定:其中NH4+质量为0.405g。试求该样品中NCl3的质量分数,该样品是否安全?(请写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下图所示的转化关系(反应条件已省略)
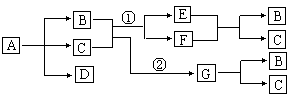
已知:B、C两种物质在不同情况下可分别发生①和②两个反应,A―G七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;且B的相对分子质量大于C。
⑴请写出下列物质的化学式:B__________;C__________;D__________;G__________。
⑵请写出E+F→B+C的化学方程式____________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
根据下图回答问题:
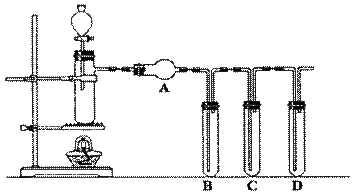
⑴装置气密性的检验须在盛放药品前进行。在上述装置中,往试管B、C、D中各加入5mL蒸馏水封住导管口,各连接处都紧密而不漏气的情况下,点燃酒精灯,微热带支管的试管一会儿,试管B、C、D中未出现气泡;熄灭酒精灯后,试管B、C、D中导管内水面也未上升,其原因是:____。
⑵①一般来说,硫酸的质量分数大于60%,就具有一定的氧化性,且越浓氧化性越强;②温度也要影响氧化性,如铜放于冷的浓硫酸中反应不明显,加热就可观察到明显现象。
甲同学利用上述装置,用实验来验证硫酸氧化性的上述结论(已知98%的浓硫酸的密度为1.84g?cm-3)。他先向试管B加入5mL品红试液,向试管C、D中各加入5mL饱和澄清石灰水;向带支管的试管中放入铜粉和3mL水,然后从分液漏斗向支管试管中滴加98%的浓硫酸10滴(约0.5mL),加热至沸腾,这时支管试管中溶液颜色是否有明显变化_____(填“无”或“有”),试用数据解释其原因____________;该同学用分液漏斗再向支管试管中加98%的浓硫酸10mL,并加热至沸腾,观察到支管试管中现象是____ _。
⑶乙同学利用上述装置来检验浓硫酸和木炭粉在加热条件下发生反应的全部产物。
①浓硫酸和木炭粉在加热条件下发生反应的化学方程式为:__________。
②要达此目的,则:
C中加入试剂的名称是_________,现象是_______________;
⑷利用上述装置探究锌与浓硫酸反应产物中有SO2和H2,D中加入试剂(名称): ;检验氢气方法 。
查看答案和解析>>
科目: 来源: 题型:
已知:双烯合成也称狄尔斯-阿德耳(Diels-Alder)反应,他们因此获得1950年的诺贝尔化学奖。如:
①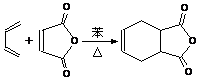
②CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
③![]()
④RCH2CH=CH2+Cl2 ![]() RCHClCH=CH2+HCl
RCHClCH=CH2+HCl
有机物 ![]() 可由烃A和酯B按下列路线合成:
可由烃A和酯B按下列路线合成:

⑴A与B反应生成C的化学方程式 。
⑵B(只含有一个碳碳双键)在RuCl作催化剂下,可由一种酯和一种炔直接加成得到,则该酯和炔结构简式分别为 和 。
⑶请用反应流程图表示以甲基-1,3-丁二烯(CH3CH=CH-CH2)、丙烯和苯合成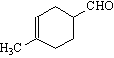 的过程。
的过程。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com