
科目: 来源: 题型:
可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
A. 锌和盐酸生成氢气
B. 二氧化锰和浓盐酸生成氯气
C. 碳酸钙和盐酸生成二氧化碳
D. 氯化钠和浓硫酸生成氯化氢
查看答案和解析>>
科目: 来源: 题型:
下列实验设计能够成功的是
|
|
|
A | 检验Na2O2试样是否变质为Na2CO3 | 向试样中加入盐酸,产生无色无味的气体 |
B | 检验某卤代烃是否是氯代烃 |
|
C | 证明酸性条件H2O2氧化性比I2强 |
|
D | 证明醋酸是弱酸 | 取醋酸钠固体加水溶解,测其pH值,pH>7 |
查看答案和解析>>
科目: 来源: 题型:
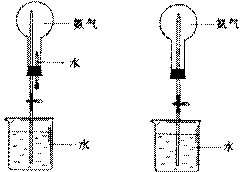
制取氨气并完成喷泉实验(图中夹持装置均已略去)。
(1)写出实验室制取氨气前化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。该实验的原理是 。
(4)如果只提供如图2的装置,请说明引发喷泉的方法
查看答案和解析>>
科目: 来源: 题型:
关于某溶液所含离子检验的方法和结论正确的是
A.加入一定量的NaOH溶液,有白色沉淀生成,则原溶液一定有Mg2+
B. 加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失则原溶液一定有Cl-
C. 加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中可能有CO32-或SO32-
D. 加入NaOH并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液是铵盐溶液。
查看答案和解析>>
科目: 来源: 题型:
下列实验操作中错误的是
A 分液时,分液漏斗下层液体从下口放出,上层液体从上层倒出
B 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C 配浓硫酸和浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中,及时搅拌和冷却
D 测溶液的PH值需先用蒸馏水润湿PH试纸,再用干燥洁净的玻璃棒蘸溶液滴在试纸上,并与标准比色卡对照
查看答案和解析>>
科目: 来源: 题型:
进行化学实验必须注意安全,下列几种处理事故的方法正确的是
①浓硫酸沾到皮肤上,先用水冲洗,再用布擦干
②苯酚洒到皮肤上,用Na2CO3 溶液洗涤
③酒精不小心洒到实验桌上,并燃烧起来,应立即用水扑灭
④误食重金属离子,喝煮沸过的鲜牛奶
⑤镁带着火应用干粉灭火器灭火,不能用泡沫灭火器
⑥实验时不慎被玻璃划破手指,引起轻微流血时,用三氯化铁溶液止血
A. 全部正确 B. 只有②③④⑤正确 C. 只有⑥ D. 全部错误
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A. 滴定管的“0”刻度在滴定管的上方
B. 先将PH试纸用蒸馏水润湿后,再测定溶液的PH
C. 测定中和热时,为了减少热量损失,不要搅拌溶液
D. 配制稀硫酸时,先在量筒中加一定体积的水,在边搅拌边慢慢加入浓硫酸
查看答案和解析>>
科目: 来源: 题型:
实验室用质量分数为98%,密度为1.84![]() 的硫酸配成1
的硫酸配成1![]() 的稀H2SO4。现实验仅需要这种硫酸240 mL。试回答下列问题:
的稀H2SO4。现实验仅需要这种硫酸240 mL。试回答下列问题:
(1)配制稀硫酸时,应选用容量为 mL的容量瓶;
(2)经计算需要 mL浓硫酸,在量取时宜选用下列量筒中的 。
A.5 mL B.10 mL C.25 mL D.50 mL
(3)配制该硫酸溶液除上述仪器外,还用到的仪器有: 。
(4)在量取浓硫酸后,进行了下列操作:
① 待稀释的硫酸温度与室温一致后,沿玻璃棒注入容量瓶中。
② 往容量瓶中小心加蒸馏水至液面接近环形标线2~3 cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
 ③ 将浓硫酸注入盛有若干毫升蒸馏水的烧杯中,并用玻璃棒搅动,使其混合均匀。
③ 将浓硫酸注入盛有若干毫升蒸馏水的烧杯中,并用玻璃棒搅动,使其混合均匀。
④ 用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。上述操作中,正确的顺序是(填序号) 。
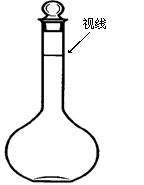
(5)某同学观察液面的情况如图所示,对所配溶液浓度有何影响?会 (填“偏高”、“偏低”、“无影响”)
(6)若出现如下错误操作,所配溶液浓度将偏高还是偏低:没有进行操作步骤④,会 ;加蒸馏水时不慎超过了刻度线,会 。(填“偏高”、“偏低”、“无影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com