
科目: 来源: 题型:
A.2.0 B.12.3 C.1.7 D.12.0
查看答案和解析>>
科目: 来源: 题型:
①pH=0的盐酸
②0.1 mol ·L-1的盐酸
③0.01 mol ·L-1的NaOH溶液
④pH=14的NaOH溶液
A.①=②=③=④ B.①>②>③>④
C.①<②<③<④ D.①=④<②<③
查看答案和解析>>
科目: 来源: 题型:
①pH=0的盐酸 ②0.1 mol ·L-1的盐酸 ③0.01 mol ·L-1的NaOH溶液 ④pH=14的NaOH溶液
A.1∶10∶100∶1 B.1∶10-1∶10-12∶10-14
C.14∶13∶12∶14 D.14∶13∶2∶1
查看答案和解析>>
科目: 来源: 题型:
材料一:现有两种一元弱酸的钠盐溶液,其物质的量浓度相等,先向这两种盐的溶液中分别通入适量的CO2,发生的反应如下:NaR+CO2+H2O![]() HR+NaHCO3,
HR+NaHCO3,
2NaR′+CO2+H2O![]() 2HR′+Na2CO3。
2HR′+Na2CO3。
材料二:碳酸钠溶液中加入过量的苯酚:
![]()
请你分析回答:
(1)在材料一中,为何在二氧化碳均适量的情况下,一份生成了NaHCO3,一份生成了Na2CO3?你能否判断出HR和HR′两种弱酸的酸性相对强弱?_____________________________________________________________________
(2)请你比较H2CO3、苯酚、![]() 三者电离程度的大小顺序。_____________________________________________________________________
三者电离程度的大小顺序。_____________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
(1)蚊虫、蚂蚁等昆虫叮咬人时常向人体血液内注入一种称之为蚁酸(主要成分为HCOOH)的有机酸,HCOOH同CH3COOH一样是一种有机弱酸,写出HCOOH在溶液中电离的方程式:___________________________________。
(2)当人受到蚂蚁叮咬时皮肤上常起小疱,这是因为人体血液中酸碱平衡被破坏所致,若不看医生治疗,过一段时间小疱也会自行痊愈,这是由于血液中又恢复了原先的酸碱平衡,试用平衡移动原理解释上述事实:_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:

图3-4
若撤去B,测知电流强度ⅠA<<ⅠC;若撤去C,并将A、B两溶液混匀后均分为两等份,再重置于电路Ⅰ、Ⅱ处,测知通过A、B混合溶液的电流强度与先前通过A溶液的电流强度的相对大小关系为:ⅠsAB>>ⅠA
已知A、B、C分别选自下列溶液:
①0.1 mol·L-1盐酸 ②0.1 mol·L-1醋酸 ③0.1 mol·L-1NaCl溶液 ④0.1 mol·L-1硫酸 ⑤0.1 mol·L-1 NaOH溶液 ⑥0.1 mol·L-1氨水,且25 ℃时,A溶液pH<7
回答下列问题:
(1)指出A、B、C是(或可能是)什么溶液?
A____________;B____________;C____________。
(2)若向C溶液中滴入酚酞试剂呈红色,则C是____________。将A、B、C分别以等体积进行两两混合,结果是哪种组合的混合液中,水的电离程度最大? ____________。(选填“A”“B”“C”)
查看答案和解析>>
科目: 来源: 题型:
A.HA+HC2-(少量) ![]() A-+H2C-
A-+H2C-
B.H2B(少量)+2A-![]() B2-+2HA
B2-+2HA
C.H2B(少量)+H2C-![]() HB-+H3C
HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中,酸性最强的是_____________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_________,最难结合质子的是____________。
(3)下列反应的离子方程式正确的是____________。
A.H3C+3A-![]() 3HA+C3- B.HB-+A-
3HA+C3- B.HB-+A-![]() HA+B2-
HA+B2-
(4)完成下列反应的离子方程式:
A.H3C+OH-(过量)____________________________________________________;
B.HA(过量)+C3-______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
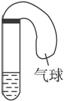
图3-3
(1)对试管以热水浴的方式加热,观察试管中的溶液,结果是__________________(有现象就写明现象的内容,无现象就写明无现象的原因,下同)。
(2)把加热后的试管放入约20 ℃的水中冷却,观察现象,试管中的溶液里有明显的现象,它是____________________________________。
查看答案和解析>>
科目: 来源: 题型:
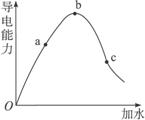
图3-2
(1)“O”点导电能力为0的理由是_________________________。
(2)a、b、c三点溶液c(H+)由小到大的顺序为________________。
(3)若使c点溶液中c(CH3COO-)增大,可采取的措施是:Ⅰ__________;Ⅱ__________;Ⅲ___________。
查看答案和解析>>
科目: 来源: 题型:
(1)向Al(OH)3沉淀中加入盐酸,沉淀溶解,其原因是________________________,有关的离子方程式为________________________。
(2)向Al(OH)3沉淀中加入苛性钠溶液,沉淀溶解,其原因是________________________,有关的离子方程式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com