
科目: 来源: 题型:
A.Na+ 1s22s22p6? B.F 1s22s22p5??
C.Cl- 1s22s22p63s23p5?? D.Ar 1s22s22p63s23p6?
查看答案和解析>>
科目: 来源: 题型:
完成下列问题:
(1)该电池的负极材料是_____________。
(2)工作时,该电池的电极反应是:负极:_____________;正极:_____________。
(3)工作时,该电池中溶液pH_____________。
查看答案和解析>>
科目: 来源: 题型:
①在25℃时,电离常数K1=3.99×10-4,K2=5.5×10-6
![]()
③1 mol A![]() 慢慢产生1.5 mol气体
慢慢产生1.5 mol气体
④A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:
(1)根据以上信息,对A的结构可作出的判断是___________________。
a.肯定有碳碳双键 b.有两个羧基
c.肯定有羧基 d.有—COOR官能团
(2)有机物A的结构简式(不含—CH3)为__________________。
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:___________________。
(4)A的一个不同类别的同分异构体是_____________________。
查看答案和解析>>
科目: 来源: 题型:
RCHO最易,R—CH2OH次之,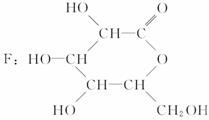 最难。
最难。
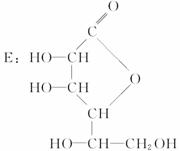
请在下列空格中填写A、B、C、D、E、F的结构简式。
A:____________;B:____________;C:____________;
D:____________;E:____________;F:____________。
查看答案和解析>>
科目: 来源: 题型:
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算a的值。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同)n(始)∶n(平)=_____________。
(4)原混合气体中,a∶b=_____________。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=_____________。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)= _____________。
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热)
2SO3(g)(正反应放热)
反应过程中SO2、O2、SO3物质的量变化如下图所示:
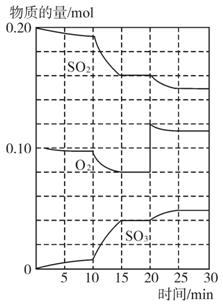
完成下列问题
(1)降低温度,SO2的转化率____________,化学反应速率____________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是____________。
(3)反应进行至20 min时,曲线发生变化的原因是____________ (用文字表达)。10 min到15 min的曲线变化的原因可能是____________ (填写编号)。
a.加了催化剂
b.缩小容器体积
c.降低温度
d.增加SO3的物质的量
查看答案和解析>>
科目: 来源: 题型:
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
最高或最低化合价 |
| +2 | +1 | +5 | +7 | +1 | +5 | +3 |
-2 |
|
| -3 | -1 |
| -3 |
|
试回答下列问题:
(1)上述元素中处于同一主族的有____________,元素②在周期表中的位置为____________。
(2)上表中某两种元素形成的分子中,每个原子都满足最外层为8电子的稳定结构,写出其电子式____________。
(3)元素①⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:__________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
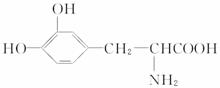
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和2001年诺贝尔化学奖的研究成果。下列关于L—多巴胺酸碱性的叙述正确的是( )
A.既没有酸性,又没有碱性 B.既具有酸性,又具有碱性
C.只有酸性,没有碱性 D.只有碱性,没有酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com