
科目: 来源: 题型:
A.2Na2O2+2H2O![]() 4NaOH+O2↑
4NaOH+O2↑
B.Mg3N2+6H2O![]() 3Mg(OH)2↓+2NH3↑
3Mg(OH)2↓+2NH3↑
C.CaC2+2H2O![]() Ca(OH)2+CH≡CH↑
Ca(OH)2+CH≡CH↑
D.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
查看答案和解析>>
科目: 来源: 题型:
A.每一个水分子内含有2个氢键
B.冰、水和水蒸气中都存在氢键
C.没有氢键就没有生命
D.H2O是一种非常稳定的化合物,这是由于氢键所致
查看答案和解析>>
科目: 来源: 题型:
A.ⅡB族 B.第八周期 C.第九周期 D.ⅥA族
查看答案和解析>>
科目: 来源: 题型:
A.1+ B.2- C.1- D.2+
查看答案和解析>>
科目: 来源: 题型:
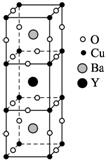
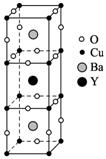
图1 图2
(1)根据所示晶胞结构,推算晶体中Y、Cu、Ba和O的原子个数比,确定其化学式。
(2)根据(1)所推出的化合物的组成,计算其中Cu原子的平均化合价(该化合物中各元素的化合价为![]() 、
、![]() 、
、![]() 和
和![]() )。试计算化合物中两种价态Cu原子个数比。
)。试计算化合物中两种价态Cu原子个数比。
(3)研究表明,当该化合物的组成为YBa2Cu3O7-x(x=0.2)时其超导性最佳。这样的组成是因结构中某些氧原子的位置出现空缺,形成晶体“缺陷”的结果。因这种组成的化合物不能用简单的整数比来表示其化学式,称为非整数比化合物。试通过计算确定化合物YBa2Cu3O7-x(x=0.2)中Cu2+与Cu3+原子个数之比。(缺陷晶体如图2所示)
查看答案和解析>>
科目: 来源: 题型:
(1)CCl3—C*HO___________________________________________
(2)HC*N_____________________________________________
(3)CH3—C*H2—COOH___________________________________
查看答案和解析>>
科目: 来源: 题型:
(1)X原子的原子结构示意图是_________________,它处于周期表中_________________周期_______________族。
(2)Z2Y2的电子式为_______________,Z2Y的电子式为_______________。
(3)XY3在标准状况下是针状晶体,它属于_______________晶体。又知XY3的水化物与Z2Y2反应可生成一种具有漂白作用的强氧化剂H2Y2,推测反应时的化学方程式为_____________
____________________________________________。
(4)Z2X属于晶体:Z2X的水溶液和XY3的水化物在溶液中反应的离子方程式是__________
____________________________________________。
(5)由X、Y、Z和氢四种元素所组成的两种化合物溶液,反应产生气体的离子方程式是
_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
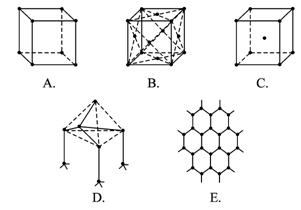
(1)代表金刚石的是(填字母编号,下同)_______________,其中每个碳原子与_______________个碳原子最接近且距离相等。金刚石属于_______________晶体。
(2)代表石墨的是_____________,其中每个正六边形占有的碳原子数平均为__________个。
(3)代表NaCl的是_______________,每个Na+周围与它最接近且距离相等的Na+有_____个。
(4)代表CsCl的是_______________,它属于晶体_______________,每个Cs+与_________个Cl-紧邻。
(5)代表干冰的是_______________,它属于_______________晶体,每个CO2分子与_________个CO2分子紧邻。
(6)若说“离子晶体中只有离子键,分子晶体中没有化学键”是否正确?简答理由。
(7)NaCl晶体、HCl晶体、干冰、金刚石熔点由高而低的顺序是_______________;其中在熔融或液态时能导电的电解质是_______________,液态不导电但为电解质的是_____________,在水溶液中能导电的非电解质是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com