
科目: 来源: 题型:
①Br2+2e-====2Br-
②2Br--2e-====Br2
③Zn-2e-====Zn2+
④Zn2++2e-====Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是
A.②和③ B.②和① C.③和① D.④和①
查看答案和解析>>
科目: 来源: 题型:
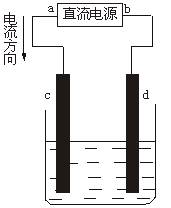
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(1)写出肼和过氧化氢的结构式:肼:___________。过氧化氢:__________________。
(2)写出热化学方程式____________________________。
(3)已知:H2O(l)==H2O(g);ΔH=+44 kJ·mol-1,则16 g液态肼与足量H2O2反应,生成氮气和水蒸气,放出的热量是___________ kJ。
(4)上述反应用于火箭推进器,除释放出大量热和快速产生大量气体外,还有一个很突出的优点________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
A.0.22 g B.0.55 g C.0.66 g D.0.44 g
查看答案和解析>>
科目: 来源: 题型:
A.40% B.50% C.80% D.90%
查看答案和解析>>
科目: 来源: 题型:
C(s)+![]() O2(g)====CO(g);ΔH=-110.35 kJ·mol-1
O2(g)====CO(g);ΔH=-110.35 kJ·mol-1
CO(g)+ ![]() O2(g)====CO2(g);ΔH=-282.57 kJ·mol-1
O2(g)====CO2(g);ΔH=-282.57 kJ·mol-1
与这些碳完全燃烧相比。损失的热量是
A.392.92 kJ B.2489.44 kJ
C.784.92 kJ D.3274.3 kJ
查看答案和解析>>
科目: 来源: 题型:
A.方程式中化学计量数表示分子数 B.该反应的ΔH2大于零
C.该反应的ΔH2=-571.6 kJ·mol-1 D.该反应可表示36 g水分解时的热效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com