
科目: 来源: 题型:
A.(NH4)3PO4
B.(NH4)2HPO4
C.NH4H2PO4
D.(NH4)2HPO4和NH4H2PO4
查看答案和解析>>
科目: 来源: 题型:
A.![]() mol B.
mol B.![]() mol
mol
C.![]() mol D.
mol D.![]() mol
mol
查看答案和解析>>
科目: 来源: 题型:
A.生石灰 B.还原铁粉
C.亚硫酸钠 D.维生素
查看答案和解析>>
科目: 来源: 题型:
2NO2+Na2CO3→NaNO2+NaNO3+CO2↑ ①
NO+NO2+Na2CO3→2NaNO2+CO2↑ ②
(1)根据反应①,每产生22.4 L(标椎状况)CO2,吸收液质量将增加__________g。
(2)配制1 000 g质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O多少克?
(3)现有1 000 g质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4 L(标准状况)CO2时,吸收液质量就增加44 g。
①计算吸收液中的NaNO2和NaNO3物质的量之比。
②1 000 g质量分数为21.2%的纯碱在20 ℃经充分吸收硝酸工业尾气后,蒸发掉688 g 水,冷却到0 ℃,最多可析出NaNO2_________________克?(0 ℃时,NaNO2的溶解度为71.2 g)
查看答案和解析>>
科目: 来源: 题型:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 255 | 385 | 459 |
生成气体/mL | 280 | 336 | 336 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?______(填“甲”或“乙”)。理由是__________。
(2)盐酸的物质的量浓度为____________。(3)Mg、Al物质的量之比为__________________。
查看答案和解析>>
科目: 来源: 题型:
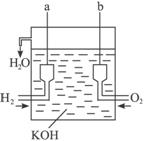
(1)a是_____极,电极反应式为_____;b是_____极,电极反应式为_____。
(2)飞船上宇航员的生活用水由燃料电池提供,已知这种电池发1度电能生成350 g水,则该电池的能量转化率为__________。
〔已知:2H2(g)+O2(g)====2H2O(l);ΔH=-572 kJ·mol-1,即每2 mol H2完全燃烧时,放出的热量为572 kJ〕
(3)这种电池的输出电压为1.2 V,要使标有“1.2 V、1.5 W”的小灯泡连续发光1小时,应消耗标准状况下H2__________L。
查看答案和解析>>
科目: 来源: 题型:
(1)降低温度,二氧化硫的转化率__________,化学反应速率__________。(填“增大”“减小”或“不变”)
(2)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如右图,反应处于平衡状态的时间是__________。
(3)据图判断,反应进行到20 min时,曲线发生变化的原因是(用文字表达)。10 min到15 min的曲线变化的原因可能是(填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com