
科目: 来源: 题型:
①平衡左移,容器内压强不一定增大 ②平衡右移,平衡时容器内压强不一定增大 ③平衡不一定移动,容器内压强一定增大 ④平衡右移,SO2转化率提高
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目: 来源: 题型:
A.由SO2和O2反应制SO3需使用催化剂
B.燃烧粉碎的黄铁矿矿石有利于SO2的生成
C.硫酸生产中用98.3%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3
D.用N2和H2合成氨需采用高压
查看答案和解析>>
科目: 来源: 题型:
A.雨水样品酸度逐渐减小
B.雨水样品酸度没有变化
C.雨水样品继续吸收空气中的CO2
D.雨水样品中的H2SO3被氧化成H2SO4
查看答案和解析>>
科目: 来源: 题型:
A.对废水、废气、废渣进行严格处理
B.不排放任何有害物质
C.在化工厂周围种草、种花、种树,使化工厂成为花园式工厂
D.以绿色植物为原料,以生物催化剂实现化工生产过程的化学
查看答案和解析>>
科目: 来源: 题型:
问题1:设空气中N2、O2的含量分别为0.80和0.20(体积分数),则110 L空气和足量的FeS2完全反应后,气体体积(同温同压)变为 L。
问题2:为了防止环境污染并对尾气进行综合利用,硫酸厂常用氨水吸收尾气中的SO2、SO3等气体,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。
为了测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00 mL,加热至120 ℃左右,使氨气全部逸出〔(NH4)2SO4和NH4HSO4的分解温度均高于200 ℃〕,测得有关实验数据如下(标准状况):
实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
1 | 3.62 | 50.00 | 0.896 |
2 | 7.24 | 50.00 | 1.792 |
3 | 10.86 | 50.00 | 2.016 |
4 | 14.48 | 50.00 | 1.568 |
(1)由1组数据直接推测:用1.81 g样品进行同样实验时,生成氨气的体积(标准状况)为 L。
(2)试计算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比为 。
(3)求所用NaOH溶液的物质的量浓度。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
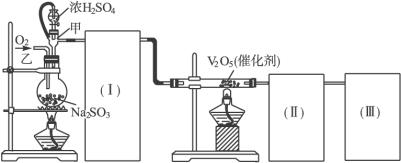
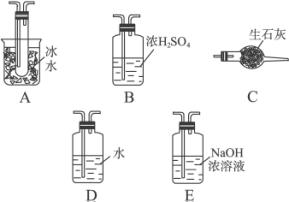
(1)根据实验的需要,(Ⅰ)(Ⅱ)(Ⅲ)处应连接合适的装置。请从下面装置中选择合适的装置,将其序号填入以下空格内:(Ⅰ) ;(Ⅱ) ;(Ⅲ) 。
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器所起作用的原理是 。
(3)用大火加热烧瓶时,SO2的转化率会 (填“提高”“不变”或“降低”)。
(4)用a mol Na2SO3粉末与足量的浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ装置增重b g,则本实验中SO2的转化率为 。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(1)写出三种设备的名称:A ,B ,C 。
(2)各设备流程中的成分是:a ,b ,c ,d ,e ,f ,g ,h ,i 。
(3)设备A中的反应方程式是 ;设备B中的反应方程式是 ;设备C中的反应方程式是 。
(4)尾气在排放到空气之前必须经过 ,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com