
科目: 来源: 题型:
A.4.6 g B.4.1 g C.6.9 g D.9.2 g
查看答案和解析>>
科目: 来源: 题型:
A.1.34 mL B.2.240 mL C.0.672 mL D.0
查看答案和解析>>
科目: 来源: 题型:
A.6∶3∶2 B.2∶3∶6 C.3∶2∶1 D.1∶2∶3
查看答案和解析>>
科目: 来源: 题型:
A.1 mol B.2 mol C.6.02×1023 D.1.204×1024
查看答案和解析>>
科目: 来源: 题型:
A.0.2 mol B.0.1 mol C.2 mol D.1 mol
查看答案和解析>>
科目: 来源: 题型:
(1)求所得滤液中溶质的质量分数。
(2)求过滤后,所得滤渣的质量。
(20 ℃,NaCl的溶解度是36 g)
查看答案和解析>>
科目: 来源: 题型:
(1)写出NaClO与KI反应的离子方程式:____________________________________。
(2)漂白液中NaClO的质量分数w(NaClO)=__________________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
2KMnO4+16HCl(浓)====2KCl+2MnCl2+5Cl2↑+8H2O
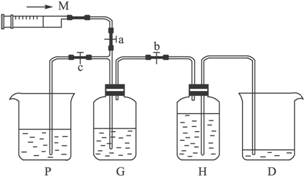
(1)装置H中盛放的试剂是_______________。
(2)尾气处理时关闭弹簧夹a和弹簧夹_________________,打开弹簧夹________________。
(3)处理尾气时,发生反应的化学方程式是___________________________________。
(4)用含0.032 mol HCl的浓盐酸跟足量高锰酸钾固体反应,产生氯气的物质的量应___________________________(填“大于”“等于”或“小于”)0.01 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com