
科目: 来源: 题型:
A.①② B.③④ C.①③④ D.②④
查看答案和解析>>
科目: 来源: 题型:
A.将FeCl3溶液滴入蒸馏水中即可
B.将FeCl3溶液滴入热水中,生成棕黄色液体即可
C.将FeCl3溶液滴入沸水中,生成红褐色液体即可
D.将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可
查看答案和解析>>
科目: 来源: 题型:
(1)向其中一支试管里滴加少量AgNO3溶液,其现象是___________________;
(2)向另一支试管里滴加少量碘水,其现象是_____________________;
(3)由上述实验得出的结论是_________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.胶体与溶液有明显不同的外观特征,呈胶状
B.胶体不稳定,静止后容易产生沉淀
C.能用渗析法净化胶体是因为胶体粒子不能透过半透膜
D.要形成胶体,必须是符合一定结构的分散质,如NaCl就不能形成胶体,只能形成溶液
查看答案和解析>>
科目: 来源: 题型:
(1)混合物中氢氧化钠的物质的量;
(2)混合物中氢氧化钾的质量分数。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量。下面是测定实验分析报告,请填写有关空白。
(1)测定目的:测定××品牌软包橙汁维生素C含量
(2)测定原理:C6H8O6+I2![]() C6H6O6+2H++2I-
C6H6O6+2H++2I-
(3)实验用品及试剂?
①仪器和用品:自选
②指示剂_______(填名称),浓度为7.50×10-3 mol·L-1标准溶液,蒸馏水。
(4)实验过程:
①洗涤仪器,检查滴定管是否漏液,润洗后装好标准溶液待用。?
②打开橙汁包装,用_______(填仪器名称),向锥形瓶中移入20.00 mL待测橙汁,滴入2滴指示剂。?
③用左手控制滴定管的________(填部位),右手摇动锥形瓶,眼睛注视_______直到滴定终点,滴定至终点的现象是___________。?
(5)数据记录与处理。(设计数据记录表格和数据处理的表格,不必填数据)若经数据处理,滴定中消耗标准碘溶液的体积是15.00 mL,则此橙汁中维生素C的含量是________mg·L-1。
(6)问题讨论:
①滴定过程中能否剧烈摇动锥形瓶?为什么??
②从分析数据看,此软包装橙汁是否是纯天然橙汁?__________(填编号)
A.是 B.可能是 C.不是
制造商可能采取的做法是_______。
A.加水稀释天然橙汁 B.橙汁已被浓缩 C.将维生素C作为添加剂?
对上述做法,你的意见是________。
A.同意 B.不同意 C.调查后再作结论
查看答案和解析>>
科目: 来源: 题型:
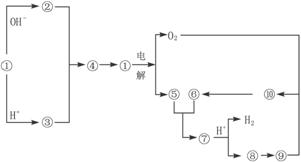
(1)①的化学式为_______,⑤和⑥反应的化学方程式为_______________________________。
(2)实验室由⑧制取⑨的离子方程式为_________,⑨转变为⑩的化学方程式为_________。由⑨转变为⑩的反应现象为___________________。
查看答案和解析>>
科目: 来源: 题型:
(1)如果V1=V2时,①m+n=13,则溶液显性_________;
②m+n=15,则溶液的Ph_____7(填“>”“=”或“<”)
(2)如果混合后pH=7时,①m+n=14,则V1/V2=___________;
②m+n=13,则V1/V2=______________。
查看答案和解析>>
科目: 来源: 题型:
(2)将单质Fe、Cu与FeCl3、FeCl2、CuCl2溶液一起放进某容器内,根据下述不同情况,填写金属或金属离子。
①充分反应后,如果Fe有剩余,则容器内不可能有________。
②充分反应后,如果容器内还有大量Fe3+,则还会有_________,一定没有_____________。
③充分反应后,如果容器内有较多Cu2+和相当量的Cu,则容器内不可能有_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com