
科目: 来源: 题型:
(1)将溶液滴在蓝色石蕊试纸上,试纸呈红色;
(2)取少量溶液,加入用稀HNO3酸化的BaCl2溶液,产生白色沉淀;
(3)将(2)中的沉淀过滤,向滤液中加入AgNO3溶液,产生白色沉淀;
(4)另取溶液,逐滴加入NaOH溶液至过量,只看到有棕色沉淀生成,且沉淀质量不减少。
由此可以推断:溶液中肯定存在的离子有__________________,溶液中肯定不存在的离子有_____________________,溶液中不能确定是否存在的离子有__________________。
查看答案和解析>>
科目: 来源: 题型:
(1)该溶液可使pH试纸呈红色;
(2)取少量该溶液加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
(3)取溶液少量加入BaCl2溶液,有白色沉淀生成,加入HNO3后沉淀不溶解;
(4)取实验(3)的上层清液,加入硝酸银溶液有白色沉淀生成,加入HNO3后沉淀不溶解;
(5)取原溶液少量加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气体放出,该气体能使润湿的红色石蕊试纸变蓝。
根据上述实验事实,溶液中肯定存在的离子有_______,肯定不存在的离子有_______,不能确定是否存在的离子有_________。
查看答案和解析>>
科目: 来源: 题型:
A.NaHSO3粉末加入HNO3溶液中

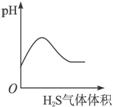
B.H2S气体通入氯水中
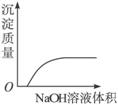
C.NaOH溶液滴入Ba(HCO3)2溶液中
D.CO2气体通入澄清石灰水中
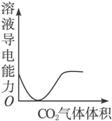
图3-8
查看答案和解析>>
科目: 来源: 题型:
A.CaCO3+2CH3COOH====(CH3COO)2Ca+H2O+CO2↑
B.SiO2+2NaOH====Na2SiO3+H2O
C.AgNO3+HCl====AgCl↓+HNO3
D.2HCl+Cu====CuCl2+H2↑
查看答案和解析>>
科目: 来源: 题型:
A.Mg、AlCl3、NaAlO2 B.KNO3、NaCl、CH3COONa
C.NaClO、Na2SO3、BaCl2 D.Ba(NO3)2、FeSO4、NH4HCO3
查看答案和解析>>
科目: 来源: 题型:
A.BaCl2溶液与Na2CO3溶液加足量稀CH3COOH
B.Ba(OH)2溶液与KNO3溶液加足量稀H2SO4
C.AgNO3溶液与Na2CO3溶液加足量稀盐酸
D.Ca(OH)2溶液与FeCl3溶液加足量稀HNO3
查看答案和解析>>
科目: 来源: 题型:阅读理解
胃是人体消化系统中的关键部位,它容纳了我们吃下的一切食物,肩负着重要的消化任务,胃通过两种途径来完成对食物的消化任务。一是利用胃黏膜分泌出的胃液(其中含有胃蛋白酶)将食物消化,例如使蛋白质降解为易于吸收的物质;二是利用胃液中的胃酸(0.2%—0.4%的盐酸),杀死食物里的细菌,确保胃和肠道的安全,同时增加胃蛋白酶的活性,帮助消化。可见胃酸对人体来说是相当重要的。
但是,人体中胃酸的量不能过多或过少,它必须控制在一定的浓度范围内(即0.2%—0.4%)。否则,当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状,严重的会降低食欲,消化不良,进而引发胃溃疡等多种形式的胃病。胃酸过少时,也会使消化作用减退,从而导致营养不良或恶性贫血。
当胃酸过多时,通常用“小苏打”“胃舒平”等药物进行治疗。小苏打的成分是碳酸氢钠,胃舒平中含有氢氧化铝。它们都能和胃液中的胃酸发生离子反应,从而中和过多的胃酸。
当胃酸过少时,医生通常给病人服用适量的酵母片促进胃液的分泌,增进食欲;也可服用适量的稀盐酸(0.3%左右),调节胃液的pH到正常范围(0.9—1.5),恢复胃的正常消化功能。
完成下列问题:
(1)写出用小苏打或胃舒平治疗胃酸过多的离子方程式。
(2)医生忠告:胃溃疡患者治疗胃酸过多时不能服用小苏打片,为什么?
(3)当进行X光透视时,医生让病人服“钡餐”(BaSO4),能否用碳酸钡代替硫酸钡?写出离子方程式并解释。(提示:Ba2+有毒)_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com