
科目: 来源: 题型:
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH3<ΔH2
C.ΔH2>ΔH1>ΔH3 D.ΔH1>ΔH3>ΔH2
查看答案和解析>>
科目: 来源: 题型:
有以下4个化学方程式:
①H2SO4(aq)+2NaOH(aq)====Na2SO4(aq)+2H2O(l)
②H2SO4(aq)+Ba(OH)2(aq)====BaSO4(s)+2H2O(l)
③NH3·H2O(aq)+HCl(aq)====NH4Cl(aq)+H2O(l)
④NH3·H2O(aq)+CH3COOH(aq)====CH3COONH4(aq)+H2O(l)
其中反应热为57.3 kJ·mol-1的是( )
A.①② B.③ C.④ D.以上都不对
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境 ③乙醇是一种再生能源 ④燃烧时放出大量热量
A.①②③ B.①②④ C.①③④ D.②③④
查看答案和解析>>
科目: 来源: 题型:
A.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热
B.强酸和强碱的稀溶液发生中和反应一定是放热反应,但弱酸和弱碱反应不一定是放热反应,所以盐类水解不一定全是吸热反应
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应
D.在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热
查看答案和解析>>
科目: 来源: 题型:
A.大于57.3 kJ B.等于57.3 kJ C.小于57.3 kJ D.无法确定
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(1)通过计算确定反应产物的组成(用化学式表示)是________,其相应的质量(g)为_______。
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH=______。
(3)写出1 mol P与O2反应生成固态P2O3的热化学方程式:___________________________。
查看答案和解析>>
科目: 来源: 题型:
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC_________Si;SiCl4_____________SiO2
(2)图3-9中立方体中心的“·”表示硅晶体中的一个原子,请在立方体的顶点用“·”表示出与之紧邻的硅原子。
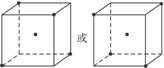
图3-9
(3)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热ΔH_______=kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com