
科目: 来源: 题型:
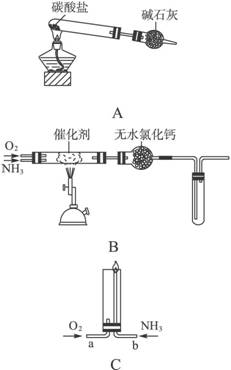
图6-14
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是___________;碱石灰的作用____________________。
(2)将产生的氨气与过量的氧气通到装置B (催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是__________试管内气体变为红棕色,该反应的化学方程式是_________________。
②停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因____________________________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是___________,其理由是______________________________。
②氨气燃烧的化学方程式是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
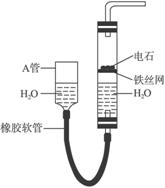
图6-13
(1)图中,A管的作用是__________________________________,制取乙炔的化学方程式是________________________________。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是____________________,乙炔发生了_________反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是_____________________,乙炔发生了__________反应。
(4)为了安全,点燃乙炔前应_______________,乙炔燃烧时的实验现象是____________________________。
查看答案和解析>>
科目: 来源: 题型:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2—3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50—80 ℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2—3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
请回答下列问题:
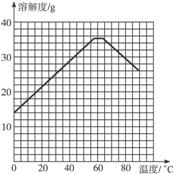
图6-11
(1)实验步骤①的目的是______________,加热的作用是__________________________。
(2)实验步骤②明显不合理,理由是_______________________________________。
(3)实验步骤④中用少量冰水洗涤晶体,其目的是________________;__________________。
(4)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O、和FeSO4·H2O。硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在57.6 ℃、64 ℃温度下可同时析出两种晶体)。
硫酸亚铁的溶解度和析出晶体的组成
温度/ ℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.03 | 0.5 | 27 | |
析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | ||||||||
请根据表中数据作出硫酸亚铁的溶解度曲线。
(5)若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为_________。
查看答案和解析>>
科目: 来源: 题型:
方法一:用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入________________________。
(2)除去蒸馏水中溶解的O2常采用__________________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是______________________________。
方法二:在图6-10中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
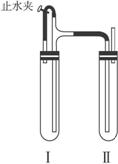
图6-10
(1)在试管Ⅰ里加入的试剂是_______________________________。
(2)在试管Ⅱ里加入的试剂是_________________________________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是__________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是________________________。
查看答案和解析>>
科目: 来源: 题型:
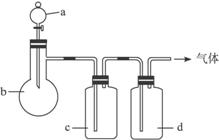
图6-9
气体 | A | b | c | d |
C2H4 | 乙醇 | 浓H2SO4 | NaOH溶液 | 浓H2SO4 |
Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓H2SO4 |
NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
NO | 稀HNO3 | 铜屑 | H2O | 浓H2SO4 |
(1)上述方法中可以得到干燥、纯净的气体是_______________(填化学式)。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)。
①气体__________,理由是____________________________________;
②气体__________,理由是_____________________________________;
③气体__________,理由是_____________________________________;
④气体__________,理由是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
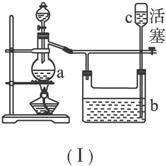

图6-8
(1)若用(Ⅰ)制取氯气,b瓶中宜加入的液体一般为________________,在选取试剂正确且适量的前提下,反应开始后,当关闭活塞时发现c中液面不明显上升,估计可能的原因是_____________________。检查原因的简单方法是______________________。
(2)若在(Ⅰ)中用Na2SO3固体与1∶1的硫酸制取SO2气体,通常可以对(Ⅰ)中制气装置进行怎样的简单改动?________________。b中的液体一般应选____________________________。
(3)装置(Ⅰ)中b瓶能防止多余气体逸散的原因是(简要回答)_________________________。
(4)用(Ⅱ)或(Ⅲ)代替(Ⅰ)中的b—c部分,是否可行?__________。简要说明理由______________________。
查看答案和解析>>
科目: 来源: 题型:
方案Ⅰ:
第一步:电解。
第二步:Fe![]() Fe2+
Fe2+![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3
方案Ⅱ:Fe![]() Fe2+
Fe2+![]() Fe3+
Fe3+![]() Fe(OH)3
Fe(OH)3
二者均过滤、洗涤、烘干。
(1)上述方案__________节约实验时间。
(2)生产同样多的产品,方案________________节约试剂。
(3)请用上述原料,设计只用两步就能完成的实验方案。
查看答案和解析>>
科目: 来源: 题型:
A.锌粒与稀HNO3反应制备H2
B.向饱和NaCl溶液中滴加浓H2SO4制备HCl
C.固体Na2SO3与浓H2SO4反应制备SO2
D.大理石与浓H2SO4反应制备CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com