
科目: 来源: 题型:
A.硫化亚铁放入盐酸中S2-+2H+====H2S↑
B.硫酸铜溶液中通入硫化氢Cu2++H2S====CuS↓+2H+
C.氯化铝溶液中加入过量氨水Al3++4NH3·H2O====![]() +4
+4![]() +2H2O
+2H2O
D.碳酸氢铵溶液中加入过量氢氧化钠溶液![]() +OH-====
+OH-====![]() +H2O
+H2O
查看答案和解析>>
科目: 来源: 题型:
A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+====Ca2++2H2O
B.钠与水的反应Na+2H2O====Na++2OH-+H2↑
C.铜片插入硝酸银溶液中Cu+Ag+====Cu2++Ag
D.大理石溶于醋酸的反应CaCO3+2CH3COOH====Ca2++2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
Ce4++Fe2+====Fe3++Ce3+
Sn2++2Fe3+====2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
查看答案和解析>>
科目: 来源: 题型:
(1)写出CH4气体不完全燃烧的热化学方程式。
(2)计算n的值。
查看答案和解析>>
科目: 来源: 题型:
2C8H18(l)+23O2(g)![]() 12CO2(g)+4CO(g)+18H2O(l)
12CO2(g)+4CO(g)+18H2O(l)
人体吸进CO后,CO与人体血红蛋白结合而引起中毒。如果每辆汽车满负荷行驶,每天约有28.5 g汽油不完全燃烧。现有某40万人口的中等城市,如达到中等发达国家水平,平均每10人拥有1辆汽车。请计算这些汽车满负荷行驶时,每天可产生多少千克CO。
查看答案和解析>>
科目: 来源: 题型:
(1)烧杯间填满碎泡沫塑料的作用是__________________;
(2)环形玻璃搅拌棒能否用环形铁质搅拌棒代替?______(填“能”或“不能”),其原因是___________________________________;

(3)为什么氢氧化钠溶液的浓度要用0.55 mol·L-1?___________________________;
实验中若改用60 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”“不相等”),若实验操作均正确,则所求中和热_________(填“相等”“不相等”);
(4)已知在稀溶液中,强酸和强碱发生中和反应生成1 mol H2O时,放出57.3 kJ的热量,则上述反应的热化学方程式为:_____________________________;
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得的结果偏低,请你分析结果偏低的原因可能是_________(填字母代号)。
a.测量盐酸的温度后,温度计没有用水冲洗干净
b.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
c.做本实验的当天室温较高
d.将50 mL 0.55 mol·L-1的氢氧化钠溶液取成了50 mL 0.55 mol·L-1的氨水
e.在量取盐酸时仰视读数
f.大烧杯的盖板中间小孔太大
查看答案和解析>>
科目: 来源: 题型:
(1)先检验________,加入________试剂(或溶液)
(2)然后检验________,加入________试剂(或溶液)。离子方程式为_________________。
(3)再检验________,加入________试剂(或溶液)。离子方程式__________________。
(4)最后检验________,加入________试剂(或溶液)。离子方程式__________________。
查看答案和解析>>
科目: 来源: 题型:
(1)取样品,加热至高温,产生一种能使澄清石灰水变浑浊的无色气体。
(2)往冷却后的固体残渣中加入足量的稀HCl,固体残渣全部溶解,同时产生一种可燃气体。
根据上述实验推断:该物质中一定含有________,一定不含有________,可能含有________。写出有关反应的化学方程式,属于氧化还原反应的,标出电子转移的方向和数目。属于离子反应的,写出离子方程式。
查看答案和解析>>
科目: 来源: 题型:
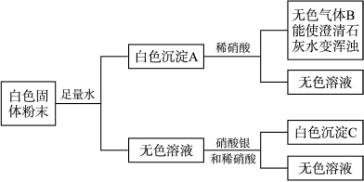
试推断(均写化学式):
A是________,B是________,C是________。白色固体粉末中一定含________一定不含________,可能含________。
查看答案和解析>>
科目: 来源: 题型:
(2)下列物质中,属于强电解质的是________(填序号,下同)。
属于弱电解质的是________。
属于非电解质的是________。
A.氯化钠 B.硫酸 C.醋酸 D.BaSO4 E.乙醇 F.蔗糖 G.水 H.三氧化硫 I.铜 J.氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com