
科目: 来源: 题型:
途径Ⅰ:C(s)+O2(g)![]() CO2(g)(放热Q1 kJ)
CO2(g)(放热Q1 kJ)
途径Ⅱ:先制水煤气:
C(s)+H2O(g)====CO(g)+H2(g)(吸热Q2 kJ)
再燃烧水煤气: (共放热Q3 kJ)
(共放热Q3 kJ)
试回答下列问题:
(1)判断两种途径放热:途径Ⅰ放出的热量__________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)Q1、Q2、Q3的数学关系式是__________________。
(3)由于制取水煤气反应里,反应物所具有的总能量_____________生成物所具有的总能量,那么在化学反应时,反应物就需要__________________能量才能转化为生成物,因此其反应条件为_________。
(4)简述煤通过途径Ⅱ作为燃料的意义_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
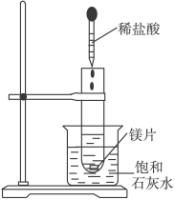
(1)实验中观察到的现象是________________________________________________。
(2)产生上述现象的原因是________________________________________________。
(3)写出有关反应的离子方程式____________________________________________。
(4)由实验推知,MgCl2溶液和H2的总能量______(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目: 来源: 题型:
H2(g)+![]() O2(g)====H2O(g);ΔH=-Q2/2 kJ·mol-1
O2(g)====H2O(g);ΔH=-Q2/2 kJ·mol-1
H2(g)+![]() O2(g)====H2O(l);ΔH=-Q3/2 kJ·mol-1
O2(g)====H2O(l);ΔH=-Q3/2 kJ·mol-1
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2 L(标准状况),经完全燃烧后,恢复到常温,则放出的热量为
A.0.4Q1+0.05 Q3 B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3 D.0.4Q1+0.2Q2
查看答案和解析>>
科目: 来源: 题型:
A.反应热指的是反应过程中放出的热量
B.热化学方程式中的化学计量数意义之一是表示分子的个数
C.在热化学方程式中无论反应物还是生成物必须标明聚集状态
D.所有的化学反应都伴随能量的变化
查看答案和解析>>
科目: 来源: 题型:
2H2(g)+O2(g)====2H2O(l);ΔH2
则关于ΔH1与ΔH2的大小比较正确的是
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法比较
查看答案和解析>>
科目: 来源: 题型:
CO(g)+1/2O2(g)====CO2(g);ΔH2=-282.57 kJ·mol-1
则:C(s)+O2(g)====CO2(g);ΔH3等于
A.+172.22 kJ·mol-1 B.-172.22 kJ·mol-1
C.+392.92 kJ·mol-1 D.-392.92 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可
B.凡是在加热或点燃条件下进行的反应都是吸热反应
C.表明反应所放出或吸收的热量的化学方程式叫做热化学方程式
D.氢气在氧气中燃烧的热化学方程式是:2H2(g)+O2(g)====2H2O(l);ΔH=-483.6 kJ
查看答案和解析>>
科目: 来源: 题型:
A.MgCO3(s)====MgO(s)+CO2(g);ΔH=+112.2 kJ
B.MgCO3(s)====MgO(s)+CO2(g);ΔH=+112.2 kJ·mol-1
C.MgCO3====MgO(s)+CO2(g);ΔH=+112.2 kJ·mol-1
D.MgCO3(s)====MgO(s)+CO2(g);ΔH=-112.2 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.质量 B.体积 C.分子数 D.物质的量
查看答案和解析>>
科目: 来源: 题型:
已知31 g白磷变成31 g红磷放出18.39 kJ热量。
4P(白,s)+5O2(g)====2P2O5(s);ΔH=-Q1。
4P(红,s)+5O2(g)====2P2O5(s);ΔH=-Q2。
以上两反应中Q1和Q2的关系是
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com