
科目: 来源: 题型:
A.因为SO2有漂白性,所以它能使品红溶液、溴水、KMnO4酸性溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂粉精、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.SO2和Cl2都有漂白作用,将两种气体同时通入湿润的有色布条,漂白效果更好
查看答案和解析>>
科目: 来源: 题型:
A.KOH和Al2(SO4)3 B.稀H2SO4和NaHCO3
C.CaCl2和Na2CO3 D.Ba(OH)2和NaHCO3
查看答案和解析>>
科目: 来源: 题型:
①酚酞试液 ②银氨溶液 ③稀H2SO4 ④FeCl3溶液(加少量HCl)
⑤氢硫酸 ⑥Cu(OH)2悬浊液 ⑦Na2CO3溶液 ⑧氯水
A.②④⑤⑧ B.①②④⑥⑧
C.②③⑤⑦ D.②⑤⑥⑧
查看答案和解析>>
科目: 来源: 题型:
A.不慎将浓碱溶液沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液
B.如果将苯酚浓溶液沾到皮肤上,应立即用酒精洗
C.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再慢慢加入浓硫酸,并不停搅拌
查看答案和解析>>
科目: 来源: 题型:
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还加入___________________________________。
(2)除去蒸馏水中溶解的O2常采用______________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是______________________________________。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。

(1)在试管Ⅰ里加入的试剂是____________________________________。
(2)在试管Ⅱ里加入的试剂是____________________________________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是___________________________________________________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是_________________________。
查看答案和解析>>
科目: 来源: 题型:

现用含少量硫化亚铁的大理石和盐酸反应制取CO2气体,实验步骤如下:
(1)将橡皮塞B塞在A烧瓶中,并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈的深度,准确称其质量为m1 g。
(2)连接制备和净化气体的装置。从F装置排出的CO2气体中,可能混有的杂质是__________,若要在A中收集纯净的CO2气体,应分别将F中排出的气体通过__________________装置(按顺序填写装置编号)。D装置中不使用Na2CO3溶液的原因是___________________________(写有关反应的离子方程式)。
(3)将导管G插入烧瓶A中用向________(填“上”或“下”)排空气法收集CO2,检验CO2气体已经充满烧瓶的方法是______________________________________________________。若经检验,CO2气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2 g。
(4)将烧瓶口的橡皮塞取下,向烧瓶内注水至标记线,再将水小心地倒入量筒,测量出水的体积可认为是CO2气体的体积,将该体积换算为标准状况时为V mL,请写出CO2相对分子质量的计算式_____________________。
若不将气体干燥和净化,测定的数值将会______________(填“偏高”“偏低”或“无影响”),理由是___________________________________________。该实验的第(4)步操作一定会使所测定的数值偏高,原因是_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
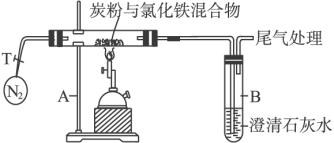
(1)设计方案:将一定量氧化铁在隔绝氧气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(2)操作步骤:①称取3.2 g氧化铁与2 g炭粉均匀混合,放入质量为48.48 g的玻璃管中按下图装置连接。②加热前先通一段时间纯净、干燥的氮气。③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊。④完全反应后,冷却至室温。称得玻璃管和固体的总质量为52.24 g。
(3)处理数据并回答问题:
①步骤②的目的是___________________________________________________。
②步骤③的现象说明__________________________________________________。
③经计算,气体产物中碳元素的质量为__________g,氧元素的质量为 _____________g。
④根据数据处理结果得出气体的成分是__________,理由是_________________________。
查看答案和解析>>
科目: 来源: 题型:
称此样品6.30 g,加入6.0 mol·L-1的硫酸至过量,产生无色气体560 mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32 g,透过蓝色钴玻璃观察,滤液的焰色反应无紫色。请根据实验填写下列空白:
(1)若用下图所示仪器组装进行上述实验,气体从左到右各仪器的正确连接顺序为_______接_______,_______接________,______接________;X溶液是_____________,汽油的作用是___________________________________________________。

(2)操作时,怎样才能正确地测出放出气体的体积?__________________________________。
(3)若实验中加入硫酸溶液的体积为5.00 mL,则样品中Na2SO3的质量分数是多少(写出计算过程)。
(4)相关离子方程式是___________________________________________________。
(5)一定含有的杂质是什么?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
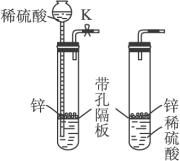
甲 乙
(1)打开止水夹K时,产生的现象是:长颈漏斗内液体流入试管,当液面与锌接触时,即产生气泡。此时,若关闭止水夹K,产生的现象是:_____________________________________。
(2)甲中长颈漏斗下端管口应处于隔板之下的理由是:_________________________________。
(3)下列物质不宜用甲装置来随制随停地制取相应气体的是_______________(填选项的标号)。
A.用CaC2(电石)制C2H2
B.用Na2SO3制SO2
C.用NaCl固体制取HCl
D.用CaCO3(大理石)制CO2
(4)用乙装置制取H2,也可达到随制随停的效果,其操作方法是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com