
科目: 来源: 题型:
A.+5 B.+
查看答案和解析>>
科目: 来源: 题型:
A.①④ B.④① C.②③ D.③②
查看答案和解析>>
科目: 来源: 题型:
AX、Y、Z、T B.Y、X、Z、T C.X、Y、T、Z D.Y、X、T、Z
查看答案和解析>>
科目: 来源: 题型:
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.金属阳离子被还原后,一定得到该元素的单质
C.核外电子总数相同的原子,一定是同种元素的原子
D.能与酸反应的氧化物,一定是碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
A.原子序数关系是Z>Y>X B.粒子半径的关系是Yn->Xn+
C.Z一定是稀有气体元素的一种原子 D.原子半径的关系是r(X)<r(Z)<r(Y)
查看答案和解析>>
科目: 来源: 题型:
A.原子半径X>Y>Z B.气态氢化物稳定性HX>H2Y>ZH3
C.非金属性X>Y>Z D.气态氢化物的还原性HX<H2Y<ZH3
查看答案和解析>>
科目: 来源: 题型:
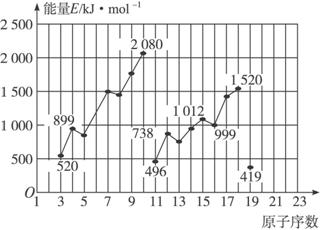
(1)同主族内不同元素的E值变化的特点是:__________________。各主族中E值的这种变化特点体现了元素性质的__________________变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象,试预测下列关系式中正确的是_________(填写编号)。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 mol气态Ca原子失去最外层一个电子所需能量E值的范围:
__________________<E<__________________。
(4)10号元素E值较大的原因是_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)氯气能从碘化钾中将碘置换出来。据此判断氯元素和碘元素非金属性的强弱。
(2)磷元素和硫元素的最高正化合价分别为+5、+6,且磷元素的非金属性弱于硫元素。请写出这两种元素最高价氧化物对应水化物的化学式,并比较它们酸性的强弱。
(3)H2SO4、H2SeO4分别是硫元素和硒元素最高正价氧化物对应的水化物,且H2SO4的酸性强于H2SeO4。据此判断硫元素和硒元素氧化能力的强弱。
(4)溴单质在加热的条件下可与氢气化合生成HBr,碘单质在高温条件下才能与氢气化合生成HI。据此判断HBr和HI稳定性的强弱。
(5)请用一个化学反应事实说明氟的非金属性强于氧,并写出相关的化学反应方程式。
(6)说明氯元素的非金属性强于溴元素的化学事实有哪些?
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(1)写出Be与NaOH溶液反应的离子方程式(生成Na2BeO2)________________________;
(2)Be(OH)2与Mg(OH)2可用试剂________鉴别,其离子方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com