
科目: 来源: 题型:
(1)方解石的失重百分比为__________。
(2)计算矿物中高岭石的质量分数。
查看答案和解析>>
科目: 来源: 题型:
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是____________________。
(2)进行Ⅰ操作时,控制溶液pH=7—8(有关氢氧化物沉淀的pH见下表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致__________溶解、__________沉淀。
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 1.5 | 3.3 | 9.4 |
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入________ (填入物质的化学式),然后____________________ (依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______(填写物质化学式)。
(5)现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量 ②高温分解 ③___________________④________________⑤MgO称量
(6)
查看答案和解析>>
科目: 来源: 题型:
①2X+O2=
上述方程式中除氧气外的其他物质均为氧化物,且通常状况下X、Y、Z都是气体,请根据要求回答问题:
(1)如果反应①在常温常压下即可顺利进行,则M的化学式是__________________________。
(2)如果反应②是一个燃烧反应,则Q的电子式是____________________,其分子为_________ (填“极性分子”或“非极性分子”)。
(3)如果反应③需在催化剂存在并加热条件下进行,则Z的化学式是___________________,其固体的晶体类型为_________。
Ⅱ.(4)将
(5)取
Ⅲ.(6)反应①—⑤是氧化还原反应,但其中一个的化合价升降与另外四个有明显不同,请你找出这个反应:_________ (填序号),你作此选择的理由是___________________________。
查看答案和解析>>
科目: 来源: 题型:
(2)温室效应导致海平面上升,引起温室效应的人为原因主要是____________________。
(3)为了控制温室效应。各国科学家提出了不少方法和设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减小大气中CO2的浓度。为使CO2液化,可采用的措施是__________。
A.减压、升温 B.增压、升温
C.减压、降温 D.增压、降温
(4)科学家研究发现,用“汽水”(一种能释放CO2的弱酸性溶液)浇灌植物能促进植物的生长。原因是它能__________。
①加强呼吸作用 ②加强光合作用 ③改良碱性土壤、调节pH ④加强植物蒸腾作用
A.①② B.②③ C.③④ D.②③④
(5)快速、有效地减缓大气中CO2大量增加的生态学措施是__________。
A.使用天然气等燃料 B.控制全球人口增长
C.植树造林,保护森林 D.立即减少煤和石油的燃烧
查看答案和解析>>
科目: 来源: 题型:
(1)X是__________,Y是__________,Z是__________。
(2)由Y和Z组成,且Y和Z的质量比为7∶20的化合物的化学式(分子式)是__________。
(3)由X、Y、Z中的两种元素组成,且与X、Z分子具有相同电子数的两种离子是__________和__________。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,该盐的化学式(分子式)是____________________。
查看答案和解析>>
科目: 来源: 题型:
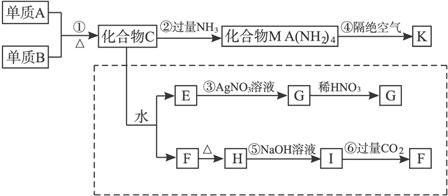
请回答下列问题:
(1)写出化学式:单质B:__________,化合物F:__________。
(2)物质H是__________晶体。
(3)写出下列反应的离子方程式:
反应③______________________________,
反应⑤______________________________,
反应⑥______________________________。
(4)写出反应②和④的化学方程式:
②___________________________________,
④___________________________________。
查看答案和解析>>
科目: 来源: 题型:
①称取样品若干,放在蒸发皿中充分加热;
②样品冷却后,倾入烧杯中用蒸馏水溶解;
③向烧杯内的溶液加入足量的BaCl2溶液,然后再加入足量的Na2CO3溶液;
④过滤;
⑤向滤液中加入稀盐酸至溶液的pH为5—6,然后将溶液加热至沸腾。试回答:
(1)操作①中反应的化学方程式为________________________________________,
判断加热已充分的方法是______________________________________________。
(2)为什么可以在加入BaCl2溶液和Na2CO3溶液后一次过滤?
(3)判断加入的Na2CO3溶液已足量的方法是____________________________________。
(4)控制加入盐酸至滤液pH在5—6的目的是_______________________________________。
(5)最后将滤液加热至沸腾的目的是____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
2KClO3+H![]() 2ClO2↑+K2SO4+2CO2↑+2H2O
2ClO2↑+K2SO4+2CO2↑+2H2O
下列说法正确的是( )
A.KClO3在反应中失去电子
B.ClO2是氧化产物
C.H
D.1 mol KClO3参加反应有2 mol电子转移
查看答案和解析>>
科目: 来源: 题型:
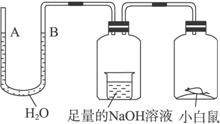
A.A处上升,B处下降 B.A、B两处都下降
C.A处下降,B处上升 D.A、B两处都不变
查看答案和解析>>
科目: 来源: 题型:
A.加入盐酸酸化了的Ba(NO3)2溶液 B.加入盐酸酸化了的BaCl2溶液
C.先加盐酸酸化,再加Ba(NO3)2溶液 D.先加盐酸酸化,再加BaCl2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com