
科目: 来源: 题型:
(1)原子半径最小的元素是__________。
(2)第一电离能最大的元素是__________。
(3)电负性最大的元素是__________。
(4)原子半径最大的元素是__________。
(5)第四周期中,第一电离能最小的元素是__________。
查看答案和解析>>
科目: 来源: 题型:
A.第一电离能Y小于X
B.气态氢化物的稳定性:HmY强于HnX
C.最高价含氧酸的酸性:X对应的酸酸性强于Y的
D.X和Y形成化合物时,X显负价,Y显正价
查看答案和解析>>
科目: 来源: 题型:
(1)试推断A、B、C、D四种元素的名称和符号。
(2)写出上述元素两两化合生成的离子化合物的化学式。
查看答案和解析>>
科目: 来源: 题型:
(1)NaF (2)AlCl3 (3)NO (4)MgO (5)BeCl2 (6)CO2
共价化合物____________________________________________________________。
离子化合物____________________________________________________________。
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
查看答案和解析>>
科目: 来源: 题型:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是____________________。
(2)判断下列物质是离子化合物还是共价化合物?
Mg3N2 BeCl2 AlCl3 SiC
查看答案和解析>>
科目: 来源: 题型:
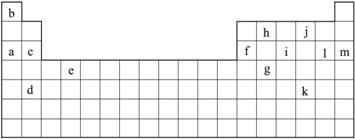
(1)下列__________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子核失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7 296 | 4 570 | 1 820 |
失去第三个电子 | 11 799 | 6 920 | 2 750 |
失去第四个电子 | — | 9 550 | 11 600 |
①通过上述信息和表中的数据分析,为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量__________________________________________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成的化合物的化学式__________。
③Y是周期表中__________族的元素。
④以上13种元素中,__________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目: 来源: 题型:
A.各原子轨道电子均已填满
B.其原子与同周期ⅠA、ⅡA族阳离子具有相同的核外电子排布?
C.化学性质很不活泼
D.同周期中第一电离能最大
查看答案和解析>>
科目: 来源: 题型:
A.同周期元素中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.室温时,零族元素的单质都是气体
D.同一周期中,碱金属元素的第一电离能最小
查看答案和解析>>
科目: 来源: 题型:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。?
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):__________,理由是___________
___________________。
(2)Y是___________,Z是______________,W是______________。
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1。写出该化合物的名称及化学式__________。
查看答案和解析>>
科目: 来源: 题型:
A.甲与乙处于同一周期
B.甲与乙处于同一主族
C.甲与乙的单质都是原子晶体
D.甲与乙的原子序数之和为偶数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com