
科目: 来源: 题型:
A.v(NH3)=0.010 mol·(L·s)-1 B.v(O2)=0.001 mol·(L·s)-1
C.v(NO)=0.0010 mol·(L·s)-1 D.v(H2O)=0.045 mol·(L·s)-1
查看答案和解析>>
科目: 来源: 题型:
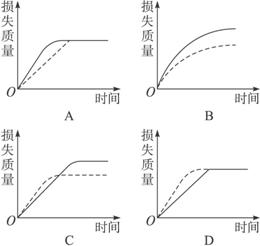
查看答案和解析>>
科目: 来源: 题型:
N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
(1)若在相同温度下,分别在
(2)若在上述定压密闭容器中,反应已达到平衡时,再加入0.5摩尔氩气,则N2的转化率会起什么变化?正反应速度与原平衡相比,有无变化,简答理由。
(3)若在
①若x=0,y=0,则z=_____________。
②若x=0.75,则y应为_____________mol、z应为_____________mol。
③x、y、z应满足的一般条件是______________________________________。
查看答案和解析>>
科目: 来源: 题型:
①H2O2+2KI+H2SO4![]() I2+K2SO4+2H2O
I2+K2SO4+2H2O
②H2O2+I2![]() 2HIO
2HIO
③H2O2+2HIO![]() I2+O2↑+2H2O
I2+O2↑+2H2O
(1)H2O2在反应③的作用是_________________。
A.氧化剂 B.还原剂
C.既是氧化剂,也是还原剂 D.既不是氧化剂,也不是还原剂
(2)有人认为②③两反应说明了碘单质是过氧化氢分解的催化剂,你认为_________________(填“对”或“不对”),理由是________________________________________________。
(3)上述反应说明H2O2、I2、HIO氧化性由强到弱的顺序是__________________________。
查看答案和解析>>
科目: 来源: 题型:
A.大于 B.小于 C.等于 D.不能确定
查看答案和解析>>
科目: 来源: 题型:
组号 | 反应温度/℃ | Na2S2O3 | H2SO4 | H2O体积/mL | ||
体积/mL | 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | |||
A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目: 来源: 题型:
(1)试配平该反应的化学方程式,并用短线标出电子转移方向及总数。
NaIO3+NaHSO3——NaHSO4+Na2SO4+I2+H2O
(2)已知含氧酸盐的氧化作用随溶液酸性的增强而增强,在制备实验时,定时取样,并用酸化的氯化钡来检测![]() 生成的量,发现开始阶段反应速率呈递增的趋势,试简述这一变化趋势发生的原因:________________________________________________________________。
生成的量,发现开始阶段反应速率呈递增的趋势,试简述这一变化趋势发生的原因:________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.![]() v(NH3)=v(O2) B.
v(NH3)=v(O2) B.![]() v(O2)=v(H2O)
v(O2)=v(H2O)
C.![]() v(NH3)=v(H2O) D.
v(NH3)=v(H2O) D.![]() v(O2)=v(NO)
v(O2)=v(NO)
查看答案和解析>>
科目: 来源: 题型:
(1)根据计算确定金属氧化物的名称。
(2)计算通电后硫酸溶液的物质的量浓度(溶液体积按100 mL计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com