
科目: 来源: 题型:
2H2(g)+O2(g)![]() 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566 kJ·mol-1
2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
当使用管道煤气的用户改用天然气后,在相同条件下燃烧等体积的燃气,理论上所获得的热值,后者大约是前者的多少倍( )
查看答案和解析>>
科目: 来源: 题型:
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-566 kJ·mol-1
2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
由等物质的量的CO和CH4的混合气体共4 mol,在上述条件下完全燃烧时释放的热量为( )
A.1 173 Kj B.1 456 kJ C.2 346 kJ D.1 780 kJ
查看答案和解析>>
科目: 来源: 题型:
A.+8Q kJ·mol-1 B.+16Q kJ·mol-1
C.-8Q kJ·mol-1 D.-16Q kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.S(s)+O2(g)![]() SO2(g),反应放出的热量大于293.23 kJ·mol-1
SO2(g),反应放出的热量大于293.23 kJ·mol-1
B.S(g)+O2(g)![]() SO2(g),反应放出的热量小于293.23 kJ·mol-1
SO2(g),反应放出的热量小于293.23 kJ·mol-1
C.1 mol SO2的键能的总和大于1 mol硫和1 mol氧气的键能之和
D.1 mol SO2的键能的总和小于1 mol硫和1 mol氧气的键能之和
查看答案和解析>>
科目: 来源: 题型:
A.ΔH1>ΔH2>ΔH3 B.ΔH2<ΔH3<ΔH
查看答案和解析>>
科目: 来源: 题型:
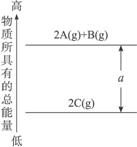
A![]()
![]()
C![]()
![]() 2A+B ΔH=a(a>0)
2A+B ΔH=a(a>0)
查看答案和解析>>
科目: 来源: 题型:
C(s)+![]() 2O2(g)
2O2(g)![]() CO(g) ΔH=-110.35 kJ·mol-1
CO(g) ΔH=-110.35 kJ·mol-1
CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH=-282.57 kJ·mol-1
CO2(g) ΔH=-282.57 kJ·mol-1
与这些炭完全燃烧相比较,损失的热量是( )
A.392.92 kJ B.2 489.44 kJ C.784.92 kJ D.3 274.3 kJ
查看答案和解析>>
科目: 来源: 题型:
在以上条件下,向体积不变的密闭容器中通入1 mol SO2和0.5 mol O2,反应达到平衡时放出热量为Q1 kJ;在同样的条件下向同样的密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量为Q2 kJ。则下列关系正确的是( )
A.2Q1=Q2 B.2Q1>Q
查看答案和解析>>
科目: 来源: 题型:
A.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol-1
B.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
C.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=-890.3 kJ
CO2(g)+2H2O(l) ΔH=-890.3 kJ
D.2H2+O2![]() 2H2O ΔH=-285.8 kJ·mol-1
2H2O ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:

A.+1 638 kJ·mol-1 B.-1 638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com