
科目: 来源: 题型:
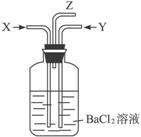
A.从Z导管出来的气体中无二氧化碳 B.气瓶中产生的沉淀是硫酸钡
C.在Z导管口有红棕色气体出现 D.气瓶中产生的沉淀是碳酸钡
查看答案和解析>>
科目: 来源: 题型:
①NO2![]() NO+O ②2NO+O2
NO+O ②2NO+O2![]() 2NO2 ③O+O2
2NO2 ③O+O2![]() O3
O3
下列对该反应过程及有关叙述正确的是( )
A.NO2起催化剂作用 B.NO起催化剂作用
C.NO2只起氧化剂作用 D.O3与O2为同一物质
查看答案和解析>>
科目: 来源: 题型:
A.NA个N2分子和NA个CO分子质量比为1∶1
B.水的摩尔质量等于NA个水分子的质量之和
C.1 mol氧气的质量等于NA个氧原子的质量
D.分别由NA个水分子组成的冰、水、水蒸气的质量各不相同
查看答案和解析>>
科目: 来源: 题型:
A.分别向其中滴加紫色的石蕊试液,现象都是先变红后褪色
B.常温下都能与铜剧烈反应
C.露置在空气中,容器中酸液的质量都增加
D.露置在空气中,容器中酸液的浓度都降低
查看答案和解析>>
科目: 来源: 题型:
A.①②③ B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目: 来源: 题型:
(1)逐滴加入6 mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6 mol·L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物
则这种白色粉末是( )
A.CaCl2·6H2O、Na2CO3 B.NaHCO3、AgNO3
C.NH4HCO3、MgCl2 D.BaCl2、MgCO3
查看答案和解析>>
科目: 来源: 题型:
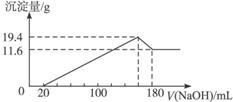
(1)原合金中Mg、Al质量各是多少?
(2)盐酸的物质的量浓度。
查看答案和解析>>
科目: 来源: 题型:
(1)白铁镀锌的作用是______________________;盖玻璃片的作用是__________________。
(2)放出气体速率由快变慢的原因是______________________________________________。
(3)为什么要加入过量NaOH溶液_______________________________________________。
(4)锌在样品中的质量分数是___________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com