
科目: 来源: 题型:
A.其单质常温下跟水反应不如Na剧烈
B.原子半径比钾小
C.碳酸盐易溶于水
D.氢氧化物不能使Al(OH)3溶解
查看答案和解析>>
科目: 来源: 题型:
①Cl<Cl-<Br- ②F-<Mg2+<Al3+ ③Na+<Na<K ④S2-<Cl-<Br-
A.①和③ B.只有② C.只有③ D.①和④
查看答案和解析>>
科目: 来源: 题型:
A.元素的化学性质随着相对原子质量的递增而呈周期性变化
B.元素周期律的实质是元素原子最外层电子数的周期性变化
C.半径由大到小、氧化性由弱到强的是K+、Mg2+、Al3+、H+,而还原性由弱到强的则是I-、Br-、Cl-、F-
D.某元素R的最高价氧化物化学式为:R2O5,又知R的气态氢化物中含氢8.8%,则R的相对原子质量为28
查看答案和解析>>
科目: 来源: 题型:
A.Na、Mg、Al最外层电子数依次增多,其简单离子的氧化性依次增强
B.P、S、Cl最高正价依次升高,对应气态氢化物稳定性增强
C.C、N、O原子半径依次增大
D.Na、K、Rb氧化物的水化物碱性依次增强
查看答案和解析>>
科目: 来源: 题型:
A.原子序数越大,原子半径一定越大
B.原子的电子层数越多,半径越大
C.元素性质的周期性变化不是元素性质的简单重复
D.按C、N、O、F的顺序,元素的最高正价依次升高
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
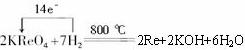
(1)根据你的理解,请说明铼元素的发现为什么会如此艰难?__________________________。
(2)铼有两种天然同位素:稳定同位素185Re和放射性同位素187Re,两种同位素原子中的中子数之和是________________。
(3)写出现代工业上用氢气还原金属铼的化学反应方程式,并标出电子转移的方向和数目____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com