
科目: 来源: 题型:
A.1s12s22p6 B.1s22s22p33s1
C.1s22s22p63s23p63d54s1 D.1s22s22p63s23p63d34s2
查看答案和解析>>
科目: 来源: 题型:
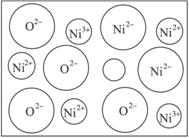
图3-40
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图340所示的缺陷:一个Ni2+空缺,另两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算晶体中Ni3+与Ni2+的离子数之比。
查看答案和解析>>
科目: 来源: 题型:
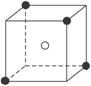
图3-39
(1)晶体中每个Y同时吸引着____________个X,每个X同时吸引着____________个Y,该晶体的化学式为____________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有____________个。
(3)晶体中距离最近的2个X与一个Y形成的夹角∠XYX为____________(填角的度数)。
(4)设该晶体的摩尔质量为M g·mol-1,晶体密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X中心间的距离为____________cm。
查看答案和解析>>
科目: 来源: 题型:
(1)由图可确定硼化镁的化学式为___________________________。
(2)请画出硼化镁的一个晶胞的透视图。标出该晶胞的面、棱、顶角上可能存在的所有硼原子和镁原子(镁原子用大白球,硼原子用小黑球表示)。
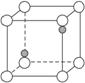
图3-38
查看答案和解析>>
科目: 来源: 题型:
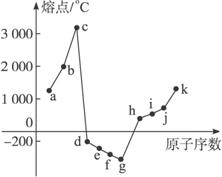
图3-37
(1)c点代表的单质可以是____________,其熔点高的主要原因是_____________________
____________________________________________________________________。
(2)d所属的晶体类型是____________________________。
查看答案和解析>>
科目: 来源: 题型:
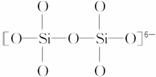
图3-36
(2)在CsCl离子晶体中距Cs+最近且等距离的Cl-个数为______________。
(3)如图3-36是石英晶体平面示意图:它实际上是立体的网状结构,其中硅、氧原子数之比为______________________。原硅酸根离子![]() 的结构表示为
的结构表示为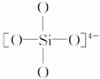 ,二聚硅酸根离子
,二聚硅酸根离子![]() 中,只有硅氧键,它的结构可表示为________________。
中,只有硅氧键,它的结构可表示为________________。
查看答案和解析>>
科目: 来源: 题型:
(1)属于原子晶体的化合物是_______________,直接由原子构成的晶体是_______________,直接由原子构成的分子晶体是_______________。
(2)由极性分子构成的晶体是_______________,含有共价键的离子晶体是_______________,属于分子晶体的单质是_______________。
(3)在一定条件下能导电而不发生化学变化的是_______________,受热熔化后化学键不发生变化的是_______________,需克服共价键的是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com