
科目: 来源: 题型:
A.V1>V2>V3
B.V1>V3>V2
C.V2>V3>V1
D.V3>V1>V2
查看答案和解析>>
科目: 来源: 题型:
A.C8H18(l)+![]() O2(g)===8CO2(g)+9H2O(g)
O2(g)===8CO2(g)+9H2O(g)
![]() =-48.40 kJ·mol-1
=-48.40 kJ·mol-1
B.C8H18(l)+![]() O2(g)===8CO2(g)+9H2O(l)
O2(g)===8CO2(g)+9H2O(l)
![]() =-5518 kJ·mol-1
=-5518 kJ·mol-1
C.C8H18 (l)+![]() O2(g)===8CO2(g)+9H2O(l)
O2(g)===8CO2(g)+9H2O(l)
![]() =+5518 kJ·mol-1
=+5518 kJ·mol-1
D.C8H18 (l)+![]() O2(g)===8CO2(g)+9H2O(l)
O2(g)===8CO2(g)+9H2O(l)
![]() =-48.40 kJ·mol-1
=-48.40 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C.除去FeCl2溶液中少的量FeCl3:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目: 来源: 题型:
A.NaOH
B.NH3·H2O
C.AgNO3
D.BaCl2
查看答案和解析>>
科目: 来源: 题型:
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0℃以上,温度越高,水的密度越小
查看答案和解析>>
科目: 来源: 题型:
(1)1 m3(标准状况)CH4按上式完全反应,产生H2________mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为________。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)/V(N2)=3∶1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
查看答案和解析>>
科目: 来源: 题型:
30.超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。
其制取原理为:Al2O3+N2+3C![]() 2AlN+3CO由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
2AlN+3CO由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
(1)称取10.00 g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出氨气3.36 L(标准状况)。
①上述反应的化学方程式为 ;
②该样品中的AlN的质量分数为________。
(2)另取10.00 g样品置于反应器中,通入2.016 L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34 g·L-1(已折算成标准状况,AlN不跟O2反应)。该样品中含杂质炭________g。
查看答案和解析>>
科目: 来源: 题型:
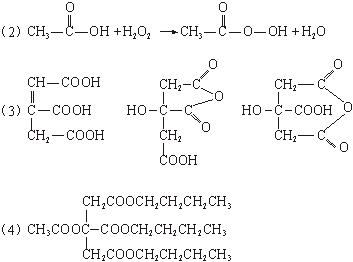
某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。

(1)CH3COOOH称为过氧乙酸,写出它的一种用途________。
(2)写出B+E→CH3COOOH+H2O的化学方程式 。
(3)写出F可能的结构简式 。
(4)写出A的结构简式 。
(5)1摩尔C分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是________。
(6)写出D跟氢溴酸(用溴化钠和浓硫酸的混合物)加热反应的化学方程式:
。
查看答案和解析>>
科目: 来源: 题型:
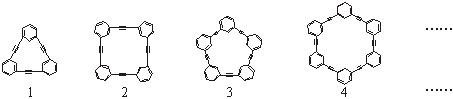
(1)上述系列中第1种物质的分子式为________。
(2)已知上述系列第1至第4种物质的分子直径在1~100 nm之间,分别将它们溶解于有机溶剂中,形成的分散系为________。
(3)以苯乙炔为基本原料,经过一定反应而得到最终产物。假设反应过程中原料无损失,理论上消耗苯乙炔与所得芳炔类大环化合物的质量比为______。
(4)在实验中,制备上述系列化合物的原料苯乙炔可用苯乙烯(![]() )为起始物质,通过加成、消去反应制得。写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选) 。
)为起始物质,通过加成、消去反应制得。写出由苯乙烯制取苯乙炔的化学方程式(所需的无机试剂自选) 。
查看答案和解析>>
科目: 来源: 题型:
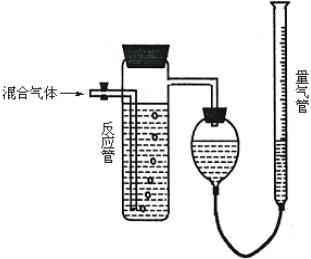
(1)混合气体进入反应管后,量气管内增加的水的体积等于________的体积(填写气体的分子式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量________(选填:偏高,偏低,不受影响)。
(3)反应管内的碘的淀粉溶液也可以用________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为C mol·L-1。N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为:________。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com