
科目: 来源: 题型:
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等
C.1 L一氧化碳气体一定比1 L氧气的质量小
D.等体积、等物质的量浓度的强酸中所含的H+数一定相等
查看答案和解析>>
科目: 来源: 题型:
A.溶液中c(H+)和c(OH-)都减小
B.溶液中c(H+)增大
C.醋酸电离平衡向左移动
D.溶液的pH增大
查看答案和解析>>
科目: 来源: 题型:
(1)H2(g)+![]() O2(g)===H2O(g) ΔH1= a kJ·mol-1
O2(g)===H2O(g) ΔH1= a kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g) ΔH2= b kJ·mol-1
(3)H2(g)+![]() O2(g)===H2O(l) ΔH3= c kJ·mol-1
O2(g)===H2O(l) ΔH3= c kJ·mol-1
(4)2H2(g)+O2(g)===2H2O(l) ΔH4= d kJ·mol-1
下列关系式中正确的是( )
A.a<c<0
B.b>d>0
C.2a=b<0
D.2c=d>0
查看答案和解析>>
科目: 来源: 题型:
A.Na2CO3 NaHCO3 NaCl NH4Cl
B.Na2CO3 NaHCO3 NH4Cl NaCl
C.(NH4)2SO4 NH4Cl NaNO3 Na2S
D.NH4Cl (NH4)2SO4 Na2S NaNO3
查看答案和解析>>
科目: 来源: 题型:
N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算a的值。
(2)反应达平衡时,混合气体的体积为716.8 L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始)∶n(平)=___________。
(4)原混合气体中,a∶b=_________________。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=________。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=___________。
查看答案和解析>>
科目: 来源: 题型:
| A | B | C | D | E | F | G |
A | — | — | — | — | — | — | ↓ |
B | — | — | — | — | ↓ | ↓ | ↓ |
C | — | — | — | ↓ | — | ↓ | ↓ |
D | — | — | ↓ | — | ↓ | ↓ | ↓ |
E | — | ↓ | — | ↓ | — | ↓ | — |
F | — | ↓ | ↓ | ↓ | ↓ | — | ↓ |
G | ↓ | ↓ | ↓ | ↓ | — | ↓ | — |
(1)A的化学式是_________________,G的化学式是_____________;
判断理由是 。
(2)写出其余几种物质的化学式:B:____________,C:____________,
D:____________,E:____________,F:_________________。
查看答案和解析>>
科目: 来源: 题型:
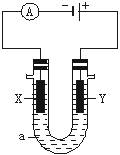
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的现象是 。
②Y电极上的电极反应式为_________________,检验该电极反应产物的方法是___________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是__________,电极反应式为 。
②Y电极的材料是__________,电极反应式为 。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目: 来源: 题型:
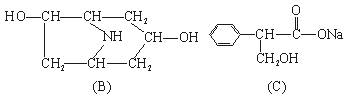
(1)A的分子式是_______________。
(2)A在NaOH水溶液中加热反应得到B和C,C是芳香化合物。B和C的结构简式是B: ,C: 。该反应属于_________________反应。
(3)温室下,C用稀盐酸酸化得到E,E的结构简式是_______________。
(4)在下列物质中,不能与E发生化学反应的是(填写序号)___________。
①浓H2SO4和浓HNO3的混合液 ②CH3CH2OH(酸催化)
③CH3CH2CH2CH3 ④Na ⑤CH3COOH(酸催化)
(5)写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①化合物是1,3,5-三取代苯
②苯环上的三个取代基分别为甲基、羟基和含有![]() 结构的基团
结构的基团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com