
科目: 来源: 题型:
Na2O | NaCl | AlF3 | AlCl3 |
920 | 801 | 1291 | 190 |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 | 2073 | -57 | 1723 |
据此作出的下列判断错误的是( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
查看答案和解析>>
科目: 来源: 题型:
A.该反应属于置换反应 B.该晶体属于原子晶体
C.该物质具有极高的熔沸点 D.该物质是一种新型化合物
查看答案和解析>>
科目: 来源: 题型:
A.离子晶体中,一定存在离子键 B.原子晶体中,只存在共价键
C.金属晶体的熔沸点均很高 D.稀有气体的原子能形成分子晶体
查看答案和解析>>
科目: 来源: 题型:
A.原子晶体中只存在非极性共价键
B.分子晶体的状态变化,只需克服分子间作用力
C.金属晶体通常具有导电、导热和良好的延展性
D.离子晶体在熔化状态下能导电
查看答案和解析>>
科目: 来源: 题型:
下面是某些短周期元素的x值:
元素符号 | Li | Be | B | C | O | F |
x值 | 0.98 | 1.57 | 2.04 | 2.25 | 3.44 | 3.98 |
元素符号 | Na | Al | Si | P | S | Cl |
x值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值变化规律,确定Mg、N的x值范围:
___________<x (Mg)< ___________,___________<x (N)< ___________。
(2)推测x值与原子半径关系是___________。根据短周期元素的x值变化特点,体现了元素性质的___________变化规律。
(3)某有机化合物结构式为:
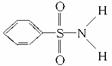 ,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的x差值(Δx)即x>1.7时,一般为离子键,Δx<1.7,一般为共价键,试推断:AlBr3中化学键类型是____________。
(5)预测元素周期表中,x值最小的元素的位置:____________(放射性元素除外)。
查看答案和解析>>
科目: 来源: 题型:

请按要求填空:
(1)G的电子式是______________;
(2)反应⑥的化学方程式是___________________________________,反应⑤在空气中发生时的现象是___________________________________,已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是_______________________________________________。
(3)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是______________。
查看答案和解析>>
科目: 来源: 题型:
(1)A、B、C、D、E的元素符号分别为_______________________________________。
(2)D、E元素可组成化合物甲,电解甲的水溶液时,反应的离子方程式为____________
___________________________________________;A、C元素可组成原子个数比为1∶1的化合物乙,将E单质通入乙的水溶液中,生成一种强酸,并有气体放出,反应的化学方程式为______________________________________________________。
(3)A、B、C、E中的任意三种元素可组成多种化合物,其中既含离子键又含共价键,且水溶液呈酸性的化合物有(写出两种化合物)____________________________。
(4)A、C、D、E中的任意三种元素可组成多种化合物,其中溶于水时能抑制水电离的化合物有(写出两种不同类别的化合物)____________________________,它们能抑制水电离的理由是___________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是
______________________________。
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:______________________________。
(3)在一定条件下,甲与O2反应的化学方程式是__________________________________。
(4)丁的元素符号是____________,它的原子结构示意图为____________。
(5)丁的氧化物的晶体结构与____________的晶体结构相似。
查看答案和解析>>
科目: 来源: 题型:
请完成下列问题:
(1)写出X、Y、Z的元素符号:
X:________________,Y:________________,Z:________________。
(2)写出Y2X对应水化物的化学式________;该水化物含有的化学键类型为________。
查看答案和解析>>
科目: 来源: 题型:
A.CaC2与水的反应属于氧化还原反应
B.CaH2在水中以Ca2+和H-形式存在
C.四种化合物化学键类型相同
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com