
科目: 来源: 题型:
A.BaSO3和BaSO4 B.BaS C.BaSO3 D.BaSO4
查看答案和解析>>
科目: 来源: 题型:
A.①②④ B.②④ C.③④ D.①②⑤
查看答案和解析>>
科目: 来源: 题型:
(1)水电离生成H3O+和OH-叫做水的自偶电离。同水一样,过氧化氢也有极弱的自偶电离,其自偶电离的电离方程式:_______________________________。
(2)由于H2O2显弱酸性,在一定条件下它能同强碱作用生成正盐或酸式盐,请写出H2O2与Ba(OH)2反应生成正盐的化学方程式:________________________________。
(3)长期使用劣质香粉,脸部可能因生成PbS而出现黑色斑点,已知PbS与下列各物质均能反应,欲除去黑色斑点,宜选用的是_________。
A.H2O2溶液 B.KMnO4溶液 C.HNO3溶液 D.漂白粉
(4)稀H2SO4不与Cu反应,但在稀H2SO4中加入H2O2后,则可使铜顺利溶解,写出该反应的化学方程式,标明电子转移的方向和数目。
(5)将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失。甲同学认为这是由于H2O2是弱酸,消耗了OH-而使红色褪去;乙同学则认为因H2O2具有氧化性,将酚酞氧化破坏其分子结构而使红色消失。试设计一个实验,检验甲、乙两位同学谁的观点正确。
查看答案和解析>>
科目: 来源: 题型:
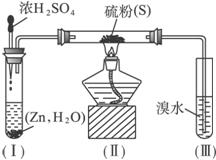
(1)将下列操作步骤补充完整:
①_____________________________________________________;
②用大火加热使硫沸腾与H2化合;
③_____________________________________________________;
④停止加热并做善后处理。
(2)装置(Ⅰ)中制氢气不直接用稀硫酸与锌反应,而将浓H2SO4滴入水中,其优点是
________________________________________________。
(3)装置(Ⅲ)中发生的现象是____________________________________,由此得出的结论是________________________,反应的离子方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:

(1)上述转化关系图中涉及的基本反应类型是_________。
(2)X、Y、Z、W的化学式依次是:X_________、Y_________、Z_________、W_________。
(3)写出X与Y、X与Z反应的化学方程式:
X+Y:__________________________________________;
X+Z:__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.Na2O2+HCl![]() NaCl+H2O2
NaCl+H2O2
B.Ag2O+H2O2![]() Ag+O2+H2O
Ag+O2+H2O
C.H2O2![]() H2O+O2(加热)
H2O+O2(加热)
D.H2O2+Cr2(SO4)3+KOH![]() K2CrO4+K2SO4+H2O
K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填序号),该反应配平的化学方程式为__________________。
(2)H2O2既体现氧化性又体现还原性的反应是________(填序号)。
(3)H2O2体现弱酸性的反应是________________(填序号),其理由是________________
________________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
过氧化氢(H2O2)又称双氧水,常温下它是一种液体,它难电离,且易分解。作为一种经典化工产品,工业上早在100多年前便开始生产。随着社会需求的增长,尤其是生态环境保护的需要,过氧化氢近年来更受到人们的青睐,并称其为绿色氧化剂。为了贮存、运输、使用的方便,工业上采用“醇析法”将其转化为固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。“醇析法”的生产工艺过程如下:在0—5 ℃下,往饱和的Na2CO3溶液中,先加入H2O2和稳定剂(MgCl2和Na2SiO3),经充分反应后,再加入异丙醇,过滤分离,即得过碳酸钠晶体。
根据上述材料,完成下列问题:
(1)依据你已有的知识,写出H2O2的结构式__________,固态时属于__________晶体。
(2)你认为H2O2被称为绿色氧化剂的主要原因是:____________________________。
(3)我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H2O2后,则可使铜顺利溶解,写出该反应的离子方程式_______________________________________。
(4)稳定剂能反应生成难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为:________
___________________________________________。
(5)加入异丙醇的作用是____________________________________________。
(6)下列物质不会使过碳酸钠失效的是______________。
A.MnO2 B.H2S C.CH3COOH D.NaHCO3
(7)向含有酚酞的NaOH溶液中滴加双氧水,溶液由红色褪至无色,主要原因是双氧水的________性。
(8)将双氧水加入经酸化的高锰酸钾溶液中,溶液的紫红色消褪了,此时双氧水表现出________性;若用H218O2的双氧水与酸化的高锰酸钾反应,18O将存在生成物________里。
(9)久置的油画,白色部位(PbSO4)常会变黑(PbS),用双氧水揩擦后又恢复原貌,有关反应的化学方程式为_________________________________。若有0.1 mol的PbS参与反应,则在此反应中发生转移的电子为________mol。
查看答案和解析>>
科目: 来源: 题型:
2HCl+H2SeO4====H2SeO3+Cl2↑+H2O
再将二氧化硫通入亚硒酸溶液中出现单质硒的沉淀。有关结论正确的是( )
A.H2SeO4的氧化性比氯气强
B.二氧化硒的还原性比二氧化硫强
C.析出1 mol硒要用H2SeO3、SO2各1 mol
D.H2SeO3的氧化性比H2SeO4强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com