
科目: 来源: 题型:
A.石蕊,由蓝变红 B.甲基橙,由黄变橙
C.酚酞,红色褪去 D.甲基橙,由橙色变黄色
查看答案和解析>>
科目: 来源: 题型:
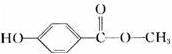 下列关于尼泊金甲酯的叙述,错误的是( )
下列关于尼泊金甲酯的叙述,错误的是( )A.分子式是C8H8O3
B.分子内所有的原子可能都在同一平面上
C.和NaOH溶液反应,1 mol尼泊金甲酯消耗2 mol NaOH
D.尼泊金甲酯的同分异构体中,苯环直接连着羟基和羧基的有10种
查看答案和解析>>
科目: 来源: 题型:
A.量筒 B.量杯 C.滴定管 D.容量瓶
查看答案和解析>>
科目: 来源: 题型:
A.等于25 Ml B.大于25 mL
C.小于25 mL D.无法判断
查看答案和解析>>
科目: 来源: 题型:
A.b、c、e、k B.c、j、k、m
C.b、h、j、m D.e、g、i、k
查看答案和解析>>
科目: 来源: 题型:
(1)若溶液中只溶解了一种溶质,则该溶质是_______________。
(2)若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则含有的溶质是___________。
(3)若溶液是由体积相等的NaOH溶液和CH3COOH溶液混合而成,且恰好呈中性,则混合前c(CH3COOH)________c(NaOH)(填“<”“>”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
(1)上述两种解释中_________(填“甲”或“乙”)正确。
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的_________(填写编号),然后测定溶液的pH。
A.固体CH3COOK B.固体CH3COONH4
C.气体NH3 D.固体NaHCO3
(3)若_________(填“甲”或“乙”)的解释正确,溶液的pH应_________(填“增大”“减小”或“ 不变”)。(已知25 ℃时,CH3COONH4溶液呈中性)
(4)常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液。判断:
①溶液中共有_________种粒子。
②溶液中有两种粒子的物质的量的和一定等于0.010 mol,它们是_________和_________。
③溶液中n(CH3COO-)+n(OH-)-n(H+)=_________mol。
查看答案和解析>>
科目: 来源: 题型:
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是________(填编号)。
(2)当上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,其pH变化最大的是________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,无气体产生的是________(填编号)。
(4)将上述①②③④这四种电解质溶液混合,发生反应的离子方程式为______________。
查看答案和解析>>
科目: 来源: 题型:
(1)在所给5种物质与水反应的产物中,属于最高价氧化物对应水化物的是________,属于无氧酸的是________。
(2)分别将0.01 mol这5种物质放入0.1 L水中反应,结果使溶液的pH接近3的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com