
科目: 来源: 题型:
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
查看答案和解析>>
科目: 来源: 题型:
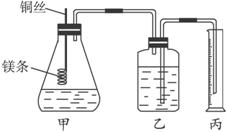
该实验主要操作步骤为:①用砂纸擦去镁条表面的氧化膜,称得质量为a g,系于铜丝末端;②锥形瓶中加有适量的稀硫酸,广口瓶中装有足量的水,连接好装置;③检查装置气密性;④把铜丝向下插入,使镁条完全浸入稀硫酸中至镁条完全溶解;⑤恢复到室温,正确操作读出量筒中水的体积为b mL。
请完成下列问题:
(1)用文字表述步骤③检查该装置气密性的操作与观察方法________________。
(2)本实验除了数据a、b外,还需要测定的其他数据有________________。
(3)如果镁条表面的氧化膜未除去,会导致实验结果________(填“偏大”“偏小”或“不变”)。
(4)若实验是在101 kPa、25 ℃下进行的,水蒸气的影响忽略不计,此时气体摩尔体积约为24.0 L·mol-1,镁原子的摩尔质量的计算式为(可不必简化):M(Mg)=_________。
查看答案和解析>>
科目: 来源: 题型:
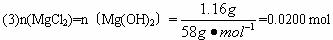
试完成下列问题:
(1)A点的沉淀物的化学式为____________,理由是______________________。
(2)写出A点到B点发生反应的离子方程式_____________________________。
(3)原混合物中MgCl2的质量是________g。AlCl3的质量是________g,NaOH的质量是________g。
(4)C点HCl溶液的体积为________mL。
查看答案和解析>>
科目: 来源: 题型:
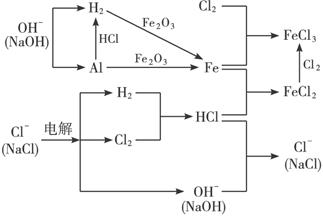
(1)向沸腾的蒸馏水中滴加A的饱和溶液,可以得到红褐色液体。A的化学式是________。
(2)将NaOH溶液注入新制备的B溶液,观察到的现象是________(选填序号)。①生成白色沉淀 ②生成血红色沉淀 ③生成红褐色沉淀 ④生成蓝色沉淀 ⑤生成白色沉淀,迅速变成灰绿色沉淀,最后变成红褐色沉淀
(3)C溶液电解的离子方程式是______________________________________。
(4)化合物F中含有组成单质N的元素,且该元素的质量分数为70%。化合物F和单质Y反应的化学方程式是______________________________________。
(5)组成单质N的元素和碳的合金在潮湿的空气中容易腐蚀。发生腐蚀时,正极的电极反应式是________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)上述事实说明了什么问题?
(2)1989年世界卫生组织把铝确定为食品污染源之一,每日摄入量应控制在4 mg以下,问铝元素含量较多会引发什么疾病?
(3)油条是我国北方常见食品之一,油条的制作口诀是“一碱、二矾、三钱盐”,其中的“碱”“矾”和“盐”分别指什么物质?写出炸油条时“矾”和“碱”之间反应的化学方程式。
(4)炸油条时1 kg面粉需加0.51 kg水、4 g“矾”、10 g“碱”和“盐”等辅料。若在烹炸过程中质量减少20%,试通过计算说明100 g油条中的含铝量是否超过安全摄入量?
(5)因铝在人体内积累有害健康,因此市场上已有“无铝发泡剂”商品出售,这类发泡剂仍是CO2发泡,如NaH2PO4和小苏打便是其中的一种。“无铝发泡剂”的发泡原理是________________________________(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
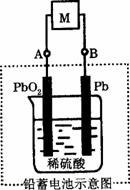
A.放电时,电流方向由B过M到A
B.充电时,铅蓄电池的正极应与充电器电源的负极相连
C.放电时,正极反应是Pb-2e-+![]() ====PbSO4
====PbSO4
D.充电时,阳极反应是PbSO4-2e-+2H2O====PbO2+![]() +4H+
+4H+
查看答案和解析>>
科目: 来源: 题型:
A.300 mL B.500 mL C.1000 mL D.1500 mL
查看答案和解析>>
科目: 来源: 题型:
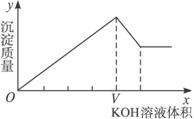
A.1∶1 B.1∶2 C.1∶3 D.2∶1
查看答案和解析>>
科目: 来源: 题型:
A.W2>W1>W3 B.W1=W2>W3
C.W1=W2=W3 D.W3>W2>W1
查看答案和解析>>
科目: 来源: 题型:
A.锌 B.铁 C.铝 D.镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com