
科目: 来源: 题型:
X极:CH4+10OH--8e-====![]() +7H2O
+7H2O
Y极:4H2O+2O2+8e-====8OH-
关于此燃料电池的说法,错误的是…( )
A.X极为负极,Y极为正极
B.工作一段时间后KOH的物质的量不变
C.在标准状况下通过5.6 L O2完全反应则有1.0 mol电子发生转移
D.该电池工作时甲烷一极附近溶液pH下降
查看答案和解析>>
科目: 来源: 题型:
A.电解水制取氢气是理想而经济的制氢方法
B.发展氢燃料电池汽车不需要安全高效的储氢技术
C.氢燃料电池汽车的使用可以有效减少城市空气污染
D.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能
查看答案和解析>>
科目: 来源: 题型:
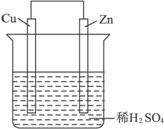
卡片NO:58 Date:2006.2.8 实验后的记录: ①Zn为阳极,Cu为阴极。 ②H+向负极移动。 ③电子流动方向为Zn→Cu。 ④Cu极有H2产生。 ⑤若有1 mol电子流过导线,则产生H2为0.5 mol。 ⑥正极电极反应式:Zn-2e-====Zn2+。 |
在卡片上,描述合理的是( )
A.①②③ B.③④⑤ C.④⑤⑥ D.②③④
查看答案和解析>>
科目: 来源: 题型:
A.电解时在阳极得到氯气,在阴极得到金属钠
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色
C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
A.Na2SO4和CuSO4 B.CuO
C.Na2O和CuO D.H2O和CuSO4
查看答案和解析>>
科目: 来源: 题型:
反应形成的固体混合物(Fe2O3、FeO)中,元素铁和氧的质量比用m(Fe)∶m(O)表示。
(1)上述固体混合物中,m(Fe)∶m(O)不可能是________(填序号,多选扣分)。
a.21∶9 b.21∶7.5 c.21∶6
(2)若m(Fe)∶m(O)=21∶8,计算Fe2O3被CO还原的质量分数。
(3)设Fe2O3被CO还原的质量分数为A%,则A%和混合物中m(Fe)∶m(O)的关系式为〔用含m(Fe)、m(O)的代数式表示〕。
A%=________________。
(4)如果Fe2O3和CO的反应分两步进行:
3Fe2O3+CO====2Fe3O4+CO2
Fe3O4+CO====3FeO+CO2
试分析反应形成的固体混合物可能的组成及相应的m(Fe)∶m(O)〔令m(Fe)∶m(O)=21∶a,写出a的取值范围〕。将结果填入下表。
混合物组成(用化学式表示) | a的取值范围 |
|
|
查看答案和解析>>
科目: 来源: 题型:
(1)写出电解制取Ca、Mg的反应方程式:____________________________________、_________________________________________。
(2)钾却不能用电解熔融的KCl方法制备,因为金属钾易溶解在熔融的KCl中而有危险,可利用Na+KCl![]() NaCl+K↑来制备钾。参考下表数据回答问题。
NaCl+K↑来制备钾。参考下表数据回答问题。
物质 | MgO | Al2O3 | MgCl2 | AlCl3 | Na | K | NaCl | KCl |
熔点/℃ | 2852 | 2072 | 714 | 190(2.5×105Pa) | 97.8 | 63.7 | 801 | 770 |
沸点/℃ | 3600 | 2982 | 1412 | 182.7 | 883 | 774 | 1413 | 1500 |
①该反应适宜选择在什么温度范围内进行?
②该反应主要应用什么化学原理?
(3)Al的制备不能用电解熔融AlCl3的方法,而采用电解熔融Al2O3的方法,请回答以下问题:
①为什么不直接电解AlCl3?
②工业上为什么不用Na还原AlCl3制备Al?
③电解Al2O3时,为什么还要加冰晶石(助熔剂)?
(4)工业上常用电解熔融MgCl2的方法生产Mg,为什么不用电解熔融MgO的方法生产Mg?
查看答案和解析>>
科目: 来源: 题型:
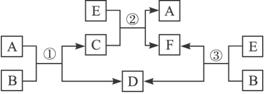
(1)若反应①②③均为水溶液中的置换反应,A、D、E为卤素单质,则A、D、E的氧化性由强到弱的顺序为________________,其中A的化学式是________________。
(2)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应①的化学方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:
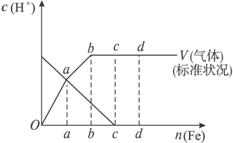
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时反应的化学方程式:
□Fe+□HNO3——□Fe(NO3)3+□![]() +□H2O
+□H2O
(2)判断从O点到a点时的还原产物,应为________。
(3)a点到b点时产生的还原产物为,其原因是________________________________。
(4)已知到达d点时反应完全结束,此时溶液中的主要阳离子为________。分析投入金属铁的物质的量之比![]() =_____________。
=_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com