
科目: 来源: 题型:
①取440 mL甲溶液与120 mL乙溶液反应,也产生1.56 g 沉淀。
②取120 mL甲溶液与440 mL乙溶液反应,产生1.56 g 沉淀。
③取120 mL甲溶液与400 mL乙溶液反应,产生3.12 g 沉淀。
通过必要的计算和推理判定:
(1)甲溶液为____________溶液,其物质的量浓度为____________ mol·L-1;乙溶液为______________溶液,其物质的量浓度为______________mol·L-1。
(2)写出实验③的有关离子方程式__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A.1 000 mL B.500 mL C.100 mL D.1 500 mL
查看答案和解析>>
科目: 来源: 题型:
A.镁不与任何金属氧化物反应,而铝可用于冶炼金属
B.金属镁、铝作电极构成原电池时,负极反应一定为:Mg-2e-====Mg2+
C.MgCl2及AlCl3溶液分别蒸发并灼热,均可得到氧化镁和氧化铝
D.历史上曾用反应:3Na+AlCl3![]() Al+3NaCl制铝;现代工业用反应:Mg+2RbCl
Al+3NaCl制铝;现代工业用反应:Mg+2RbCl![]()
MgCl2+2Rb↑,所以活动性:Mg>Rb>Na>Al
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
A.都可以用 B.只能用③
C.可以用①和② D.可以用②和③
查看答案和解析>>
科目: 来源: 题型:
A.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定
B.玻璃导管蘸水后,边旋转边向橡皮管中插入
C.加热坩埚中的硫酸铜晶体,失水后须在干燥器中冷却,再称量
D.玻璃棒蘸取溶液滴到放在表面皿上的pH试纸上
查看答案和解析>>
科目: 来源: 题型:
(1)FeSO4·7H2O的质量分数____________________。
(2)简述磷酸的作用__________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2![]() +5
+5![]() +H+====2Mn2++5
+H+====2Mn2++5![]() +3H2O
+3H2O
填空完成问题:
(1)该滴定实验所需仪器有下列中的____________________。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL) C.量筒(10 mL) D.锥形瓶E.铁架台 F.滴定管夹 G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(2)不用____(酸、碱)式滴定管盛放高锰酸钾溶液。试分析原因:________________________。
(3)选何种指示剂,说明理由___________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积__________(多、少)。根据(b-a)mL计算得到的待测浓度,比实际浓度_____________(大、小)。
查看答案和解析>>
科目: 来源: 题型:
A.可以测 B.不能测定
若选择A,试完成下列问题(则无需回答有关B的问题):
(1)指出所选用的试剂(写编号):___________________;
(2)简述操作步骤:______________________________________________________。
若选择B,试完成下列问题(则无需回答有关A的问题):
(1)试说明不能测定的原因。_____________________________________________________。
(2)你若想完成这个测定,应怎样操作?
查看答案和解析>>
科目: 来源: 题型:
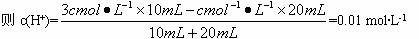
图10-2
| A | B | C | D |
盐酸的浓度/mol·L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
NaOH的浓度/mol·L-1 | 0.04 | 0.12 | 0.09 | 0.03 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com