
科目: 来源: 题型:
A.NaNO3 B.KNO3 C.KMnO4 D.I2
查看答案和解析>>
科目: 来源: 题型:
A.纯碱 B.白酒 C.白糖 D.食醋
查看答案和解析>>
科目: 来源: 题型:
A.饱和H2S溶液 B.Ca(HCO3)2溶液
C.Na2SO3稀溶液 D.饱和CaCl2溶液
查看答案和解析>>
科目: 来源: 题型:
实验序号 | ① | ② | ③ | ④ |
稀硝酸体积 | 100 Ml | 200 mL |
| 400 mL |
剩余固体质量 | 17.2 g | 8.00 g | 固体恰好全部溶解 | 0 |
气体体积 | 2.24 L | 4.48 L |
|
|
求:(1)计算稀硝酸的物质的量浓度。
(2)填写上表中的空格。
查看答案和解析>>
科目: 来源: 题型:
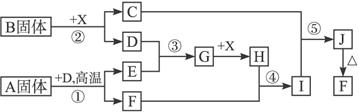
(1)化合物A中所包含的化学键有_____________________________________________。
(2)反应④的离子方程式为:___________________________________。反应⑤的化学方程式为:__________________________________。
(3)已知每生成16 g E,放出106.5 kJ的热量,则反应①的热化学方程式为:
________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)铅(Pb)的常见化合价是_______,将Pb3O4写成常见化合价的氧化物的形式为_______(已知Fe3O4可写成FeO·Fe2O3)。
(2)已知Cr的常见化合价为+2、+3、+6,Mn的常见化合价为+2、+4、+6、+7,则Cr(MnO4)2中Cr的化合价为_______,Mn的化合价为_______。
(3)Pb(N3)2在该反应中是_______剂,它的氧化产物是_______,1 mol Pb(N3)2参加反应,转移电子数是_______mol。
(4)试写出并配平这个反应的化学方程式。
![]()
查看答案和解析>>
科目: 来源: 题型:
(1)FeI2溶液中通入少量Cl2及过量Cl2时反应的离子方程式。
少量Cl2:____________________________________________。
过量Cl2:____________________________________________。
(2)已知Ca3(PO4)2、CaHPO4均不溶于水,且Ca3(PO4)2的溶解度比CaHPO4的溶解度小。将0.05 mol·L-1 Ca(H2PO4)2溶液与0.15 mol·L-1 NaOH溶液等体积混合,搅拌后静置,充分反应。请写出反应的离子方程式:_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)请写出并配平上述反应的化学方程式:____________________________________。
(2)此反应的还原剂是____________________,它的氧化产物是________________________。
(3)此反应的离子反应方程式可表示为:____________________________________。
(4)若将该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾和硫酸生成外,其他生成物还有_________________________________。
查看答案和解析>>
科目: 来源: 题型:
在一个小烧杯里,加入约20 g已研磨成粉末的氢氧化钡晶体,将小烧杯放在事先已滴有3—4滴水的玻璃片(或三合板)上,然后再加入约10 g NH4Cl晶体,并立即用玻璃棒迅速搅拌。

试完成下列问题:
(1)实验中要立即用玻璃棒迅速搅拌的原因是____________________________________ 。
(2)如果实验中没有看到“结冰”现象,可能的原因是(回答出三个或三个以上的原因)
_______________________________________________________。
(3)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热(回答出两种方案):____________________________________________________________________。
(4)实验中即使不“结冰”,将烧杯提取的时候,发现烧杯与玻璃片也“黏在一起了”。原因是____________________;试用简单的方法说明烧杯与玻片之间是因“结冰”而粘在一起的____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,ClO2、Na2FeO4、Cl2三种消毒杀菌剂的消毒效率由大到小的顺序是____________。
(2)铁酸钠之所以能净水,除它本身具有强氧化性外,另一个原因可能是_________________。
(3)二氧化氯是一种黄绿色的有刺激性气味的气体,其熔点为-59 ℃,沸点为11.0 ℃,易溶于水,ClO2可以看作是亚氯酸和氯酸的混合酸酐,工业上用稍潮湿的KClO3和草酸在60 ℃时反应制得。某学生用如图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。

请完成下列问题:
①A部分还应添加温度控制(如水浴加热)装置,B部分还应补充什么装置?_____________
______________________________________________________________。
②C中应盛放的试剂为_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com