
科目: 来源: 题型:
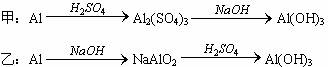
丙:
若要制得等量的Al(OH)3,则( )
A.三者消耗原料相同 B.甲消耗原料最多
C.乙消耗原料最少 D.丙消耗原料比甲少,比乙多
查看答案和解析>>
科目: 来源: 题型:
A.镓酸酸性强于铝酸 B.铝酸酸性强于镓酸
C.镓浓度小,所以不沉淀 D.Al(OH)3是难溶物
查看答案和解析>>
科目: 来源: 题型:
完成下列问题:
(1)写出溶液A中电解质的化学式。
(2)写出上述滴定反应的离子方程式。
(3)已知用于滴定的PbI2的浓度为0.009 854 mol·L-1,滴定完成时消耗掉PbI2溶液21.03 mL,则共析出金属铅多少毫克?(铅的相对原子质量为207.2,钠的相对原子质量为22.99)
查看答案和解析>>
科目: 来源: 题型:
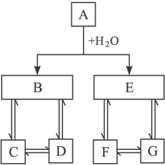
(1)写出下列物质的化学式:
A__________,D__________,E__________,G__________。
(2)写出下列反应的离子方程式:
①B→D______________________________;
②D→C______________________________;
③C+D→B______________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)根据上述实验,写出SOCl2和水反应的化学方程式:________________________。
(2)由于ZnCl2溶液蒸干灼烧后,得不到无水ZnCl2固体,只能得到ZnCl2水解的产物Zn(OH)Cl。所以,工业上往往用ZnCl2的水合晶体ZnCl2·xH2O和SOCl2混合共热来制取无水ZnCl2。在这种制法中SOCl2与晶体中结晶水反应的生成物使ZnCl2的水解被抑制,故可得无水ZnCl2。试解释灼烧过程中SOCl2抑制ZnCl2水解的原因:____________________
_________________________。
(3)SOCl2还能和某些含羟基的有机物反应,如它与乙醇的反应可表示为:
C2H5OH+SOCl2![]() C2H5Cl+SO2+HCl
C2H5Cl+SO2+HCl
和该反应相似,当过量的SOCl2跟苯甲酸混合,稍加热即发生反应,苯甲酸完全转化成一种沸点为197 ℃的液态有机物。该反应的化学方程式可表示为:_______________________。
为了使生成的有机物与混溶于其中的SOCl2分离,可以使用下列中______方法。
A.过滤 B.分液 C.蒸发结晶 D.蒸馏
查看答案和解析>>
科目: 来源: 题型:
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +H2O
+H2O![]() NH3·H2O+H+ ②
NH3·H2O+H+ ②
H++OH-![]() H2O ③
H2O ③
由于![]() 水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +OH-
+OH-![]() NH3·H2O ②
NH3·H2O ②
由于NH4Cl电离出的![]() 与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是_________(填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)你说明丙同学做出该选择的理由:______________________________。
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理_____________(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
H2A====H++HA- HA-![]() H++A2-
H++A2-
完成下列问题:
(1)Na2A溶液显__________(填“酸性”“中性”或“碱性”)。理由是__________________(用离子方程式表示)。
(2)在0.1 mol· L-1的Na2A溶液中,下列粒子浓度关系式正确的是___________。
A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1 B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1 mol·L-1NaHA溶液的pH=2,则0.1 mol·L-1 H2A溶液中氢离子的物质的量浓度可能是____________0.11 mol·L-1(填“<”“>”或“=”),理由是_____________________。
(4)0.1 mol·L-1 NaHA溶液中各种离子浓度由大到小的顺序是:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com