
科目: 来源: 题型:
方法一:将尾气通入氨水,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。已知(NH4)2SO4和NH4HSO4的分解温度均高于200 ℃,欲测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00 mL,加热至120 ℃左右,使氨气全部逸出,测得有关实验数据以下:
实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
① | 7.24 | 50.0 | 1.792 |
② | 14.48 | 50.00 | 3.584 |
③ | 21.72 | 50.00 | 4.032 |
④ | 28.96 | 50.00 | 3.136 |
(1)若取3.62 g样品用同种方法实验时,生成氨气的体积(标准状况)为__________L。
(2)该混合物中(NH4)2SO4和NH4HSO4的物质的量之比为__________。
(3)求所用NaOH溶液的物质的量浓度(写出计算过程)。
方法二:用NaOH溶液、石灰及O2吸收尾气SO2,以制取石膏(CaSO4·2H2O),此过程的中间产物是NaHSO3。实际操作中以调节尾气排放的流量来取得SO2与NaOH间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。试写出n(SO2)/n(NaOH)在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)的关系式,填入下表:
n(SO2)/n(NaOH) | n(NaHSO3) |
|
|
|
|
|
|
|
|
查看答案和解析>>
科目: 来源: 题型:
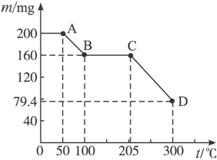
试回答下列问题:
(1)写出B点固体产物的化学式__________________;
(2)从B点到C点过程中固体物质质量不变的原因是____________________________;
(3)通过计算确定D点处产物的相对分子质量,并推断其合理的化学式。
查看答案和解析>>
科目: 来源: 题型:
(已知:R—CN![]() R—COOH;R—CH2COOHB
R—COOH;R—CH2COOHB ![]() R—CHBrCOOH)
R—CHBrCOOH)
试根据以上信息和各物质间的相互转化关系回答:
(1)写出结构简式:C______________、F______________、G______________。
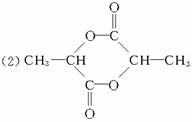
(2)2个F分子形成的环酯的结构简式:__________________________________________。
(3)写出下列反应的化学方程式:
A→B:_____________________________________________________________;
D→E:_____________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)烯烃的复分解反应就是两种烯烃交换双键两端的基团,生成两种新烯烃的反应。请写出在催化剂作用下,两个丙烯分子间发生复分解反应的化学方程式_________________。
(2)烯烃与高锰酸钾酸性溶液反应的氧化产物有如下的对应关系:
烯烃被氧化的部位 | =CH2 | RCH= |
|
氧化产物 | CO2 | R—COOH |
|
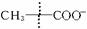
已知某烯烃的分子式为C5H10,它与高锰酸钾酸性溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是_________;若为二氧化碳和丁酮(![]() ),则此烯烃的结构简式是_____________________。
),则此烯烃的结构简式是_____________________。
查看答案和解析>>
科目: 来源: 题型:
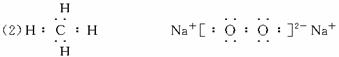
下图中,A、B、C、D、E、F在常温时均为气体,A、B分子中的电子数相同,G、H均为氧化物,其中反应生成的水及含铜化合物均略去,反应条件未注明。
试根据上图各物质间的变化回答下列问题:
(1)写出X的化学式_________________;
(2)写出物质B和G的电子式:B_________________、G_________________;
(3)反应Ⅰ的化学方程式__________________________________;
(4)反应Ⅱ的离子方程式__________________________________;
(5)在上述各步反应中,有两种物质既作氧化剂又作还原剂,它们是_________________、_________________。
查看答案和解析>>
科目: 来源: 题型:
(1)肼(N2H4)是发射航天飞船常用的高能燃料。用氨和次氯酸钠按一定物质的量之比混合反应生成肼、氯化钠和水,写出该反应的化学方程式:__________________;该反应的还原产物是__________________。
(2)在火箭推进器中分别装有肼和过氧化氢,当它们混合时即产生气体,并放出大量热。已知12.8 g液态肼与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量;1 mol液态水变成1 mol水蒸气需要吸收44 kJ的热量。写出液态肼与过氧化氢反应生成液态水的热化学方程式___________________________。
(3)新型无机非金属材料在宇航工业上有广泛应用。氮化硅(Si3N4)晶体是一种超硬、耐磨损、耐高温的物质,其晶体的类型是___________________________,化学键的类型是___________________________。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.甲同学的方案如下图所示:
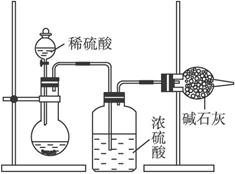
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行_________次。
(2)甲同学重复测定了三次,得到碳酸钠的质量分数的数据存在较大的偏差,你认为原因可能是_________(填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足,则可能造成误差
Ⅱ.乙同学的方案是:称取样品m g,并溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称量得固体n g。
(1)混合物中碳酸钠的质量分数为(用m、n表示) ___________________________。
(2)洗涤沉淀的操作要点是___________________________。
(3)Ca2+、Ba2+都可以使![]() 沉淀完全,但乙同学使用氯化钡溶液而不用氯化钙溶液的原因是___________________________;测定
沉淀完全,但乙同学使用氯化钡溶液而不用氯化钙溶液的原因是___________________________;测定![]() 的量,若使用氢氧化钡溶液而不用氢氧化钙溶液,结果将具有更高的精确度,原因是___________________________。
的量,若使用氢氧化钡溶液而不用氢氧化钙溶液,结果将具有更高的精确度,原因是___________________________。
查看答案和解析>>
科目: 来源: 题型:
A.附着于试管内壁的苯酚,可用碱液洗涤
B.用结晶法可以除去硝酸钾中混有的少量氯化钠
C.切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割
D.实验时,不慎打翻燃着的酒精灯,可立即用湿抹布盖灭火焰
E.浓硫酸不小心沾到皮肤上,立刻用稀烧碱溶液洗涤
F.在氢氧化铁胶体中滴加少量稀硫酸会产生沉淀
(2)下表是某种常见金属的部分性质:
颜色状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
银白色固体 | 较软 | 2.70 g·cm-3 | 660.4 ℃ | 良好 | 良好 | 良好 |
将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体。试回答:
①推断该金属可能的一种用途__________,该金属的活动性比铜__________(填“强”或“弱”)。
②请自选试剂,设计不同的实验探究该金属与铁的活动性强弱,并完成下表:
猜想 | 验证方法 | 预测实验现象 |
该金属比铁活泼 |
|
|
该金属活泼性比铁弱 |
|
|
查看答案和解析>>
科目: 来源: 题型:
A.一定没有Na2CO3和Ba(NO3)2
B.一定有Na2CO3而没有Ba(NO3)2
C.没有Ba(NO3)2但有KNO3,可能还有Na2CO3
D.没有Na2CO3但有Ba(NO3)2和KNO3
查看答案和解析>>
科目: 来源: 题型:
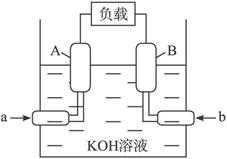
A.用多孔碳作电极是为了增大气体与溶液的接触面积
B.若b处通入的气体为氧气,则B极为正极
C.若有2 mol电子发生转移,则消耗的O2为5.6 L(标准状况)
D.放电一段时间后正极附近溶液的c(H+)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com