
科目: 来源: 题型:
A.Zn(s)+CuSO4(aq)====ZnSO4(aq)+Cu(s);ΔH=-216 kJ·mol-1,E反应物<E生成物
B.CaCO3(s)====CaO(s)+CO2(g);ΔH=+178.5 kJ·mol-1,E生成物>E反应物
C.HI(g)=![]() H2(g)+
H2(g)+![]() I2(s);ΔH=-26.5 kJ·mol-1,1 mol HI在密闭容器中分解达平衡后放出26.5 kJ的能量
I2(s);ΔH=-26.5 kJ·mol-1,1 mol HI在密闭容器中分解达平衡后放出26.5 kJ的能量
D.H+(aq)+OH-(aq)====H2O(l);ΔH=-57.2 kJ·mol-1,含1 L 1 mol·L-1的NaOH溶液与含0.5 mol H2SO4的浓硫酸混合后放热57.2 kJ
查看答案和解析>>
科目: 来源: 题型:
A.苯酚溶液不慎沾到皮肤上,应立即用稀NaOH溶液洗涤
B.液氯不能用钢瓶贮存
C.用饱和NaHCO3溶液可以除去CO2气体中混有的少量SO2
D.实验室中所有药品使用后均不能放回原瓶
查看答案和解析>>
科目: 来源: 题型:
A.铅笔芯的原料是重金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒
B.CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收CO,防止煤气中毒
C.油条制作中常常加入明矾,不仅作为膨化剂,还有利于补充人体所需的微量元素
D.薯片、薯条等淀粉类油炸食品中丙烯酰胺(CH2CHCONH2)含量较高,应谨慎食用
查看答案和解析>>
科目: 来源: 题型:
A.高温蒸煮 B.用纯净水多次洗涤 C.双氧水 D.过氧乙酸
查看答案和解析>>
科目: 来源: 题型:
2NO2+2NaOH====NaNO2+NaNO3+H2O
NO2+NO+2NaOH====2NaNO2+H2O
(1)若在标准状况下有NO、NO2的混合物恰好与50 mL 2.0 mol·L-1的NaOH溶液反应完全,且生成NaNO2和NaNO3的物质的量的比值为4∶1,则在混合气体中NO气体的体积分数为多少?
(2)设NO、NO2的混合气体用NOx表示,用碱液吸收,生成硝酸钠及亚硝酸钠再结晶分离。若生产每吨硝酸钠的成本为0.16万元,生产每吨亚硝酸钠的成本为0.27万元。目前市场出售价,硝酸钠每吨0.18万元,亚硝酸钠每吨0.28万元。则每处理22.4×109 L(标准状况)含NOx(x≥1.5)0.1%(体积分数)的尾气,所得利润y(出售价减去成本价,单位:万元)与x的关系为______________。(附解题过程)
(3)根据(2)的计算结果,在以下坐标系中作出其示意图。
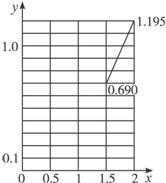
查看答案和解析>>
科目: 来源: 题型:
时间 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | a |
c(NO2)/mol·L-1 | 0 | 0.060 | c2 | 0.12 | 0.12 |
试填空:
(1)该反应的化学方程式为__________________;达到平衡时N2O4的转化率为__________,表中c2__________c3__________a(选填“>”“<”或“=”=
(2)20 s时N2O4的物质的量浓度c1=__________mol·L-1,在0—40 s内NO2的平均反应速率为__________mol·L-1·s-1
(3)若在相同情况下最初向该容器充入的是NO2气体,要达到上述同样的平衡状态,NO2的起始浓度是__________mol·L-1
查看答案和解析>>
科目: 来源: 题型:
已知:(1)凡与醛基直接相连的碳原子上的氢称为αH原子,在稀碱溶液的催化作用下,一个醛分子上的αH原子连接到另一个醛分子的氧原子上,其余部分连接到羰基碳原子上生成羟基醛,如:
R—CH2—CHO+R1—CH2—CHO![]()

(2)2R—CH2—Cl+2Na![]() R—CH2—CH2—R+2NaCl
R—CH2—CH2—R+2NaCl
(3)CH3—CH=CH2+H—Cl![]()
![]()
合成路线如下:

(1)在反应②—⑦中,属于加成反应的是____________,属于消去反应的是____________。
(2)写出下列反应方程式
E![]() F:_________________________________________________________。
F:_________________________________________________________。
H![]() G:_________________________________________________________。
G:_________________________________________________________。
(3)H也能与NaOH溶液反应,其反应方程式为__________________,生成的有机物能否在Cu或Ag作催化剂的条件下被空气氧化__________(填“能”或“否”)。
查看答案和解析>>
科目: 来源: 题型:
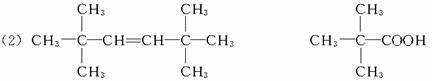
试写出:
(1)A的分子式____________________。
(2)化合物A和C的结构简式:
A________________,C________________。
(3)与C同类的同分异构体(含C)___________有种。
查看答案和解析>>
科目: 来源: 题型:
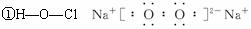
常温下,A、F为金属单质,F既能与L溶液反应,又能与N溶液反应。C、H、M为气体单质,其中H呈黄绿色,A、B、I、K、L、R焰色反应呈黄色。请回答:
①P的结构式为__________________,B的电子式为:__________________
②R水溶液呈碱性的原因可用离子方程式表示为____________________________________。
③还有一种物质能与B反应生成C,写出这个反应的化学方程式_______________________。
④还有一种物质能与J反应生成C,写出这个反应的化学方程式_______________________。
⑤某气体Q具有漂白作用,将Q与H等物质的量通入水中所得溶液没有漂白作用,写出发生的离子反应方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
钒元素广泛分散于各种矿物中,钾钒铀矿的主要成分可用化学式表示为K2H6U2V2O15,测定其中钒元素含量的方法是:先把矿石中的钒元素转化为V2O5(钒元素的化合价不变),V2O5在酸性溶液里转化为![]() ,再用草酸等测定钒。总反应可表示为:
,再用草酸等测定钒。总反应可表示为:
![]() +H2C2O4+H+
+H2C2O4+H+![]() VO2++CO2+H2O请将它配平。
VO2++CO2+H2O请将它配平。
现有钾钒铀矿样品10.2 g,用上述方法来测定钒的含量,结果消耗0.9 g草酸,那么此钾钒铀矿中钒元素的质量分数是______________。若用氧化物的形式表示钾钒铀矿的主要成分,其化学式为____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com