
科目: 来源: 题型:
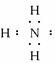
请按要求回答:
(1)写出A的化学式______________,H的电子式______________。
(2)反应⑤进行的条件是______________________________。
(3)将少量的D气体通入足量的NaOH溶液的离子反应方程式为______________________________。
(4)反应③的化学方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
H |
|
|
|
|
|
| He |
1.312 0 |
|
|
|
|
|
| 0.372 3 |
Li | Be | B | C | N | O | F | Ne |
0.520 3 | 0.899 5 | 0.800 1 | 1.086 4 | 1.402 3 | 1.314 0 | 1.681 0 | 2.080 7 |
Na | Mg | Al | Si | P | S | Cl | Ar |
0.495 8 | 0.737 7 | 0.577 6 | 0.786 5 | 1.011 8 | 0.999 6 | 1.251 1 | 1.520 5 |
K | Ca | Ga | Ge | As | Se | Br | Kr |
0.418 9 | 0.589 8 | 0.578 8 | x | 0.944 0 | 0.940 9 | 1.139 9 | 1.350 7 |
Rb | Sr | In | Sn | Sb | Te | I | Xe |
0.403 0 | 0.549 5 | 0.558 3 | 0.708 6 | 0.831 6 | 0.869 3 | 1.008 4 | 1.170 4 |
Cs | Ba | Tl | Pb | Bi | Po | At | Rn |
0.376 | 0.503 | 0.589 | 0.716 | 0.703 | 0.812 | 0.912 | 1.037 |
回答下列问题:
(1)从表中数据可知,同一主族元素原子的第一电离能I1变化规律是__________。说明同一主族元素从上到下__________能力逐渐增强。
(2)从表中数据预测Ge元素第一电离能x的取值范围_______________。
(3)观察第2、3周期中各元素的第一电离能,找出同一周期中元素第一电离能的变化规律。(说出一点即可)_______________。
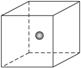
(4)SiC是原子晶体,其结构类似金刚石,为C、Si两原子依次相同排列的正四面体空间网状结构。如图为一个正方体,其中心为Si原子,试在正方体的顶点画出与Si(用![]() 表示)最近的C(用
表示)最近的C(用![]() 表示)的位置。
表示)的位置。
查看答案和解析>>
科目: 来源: 题型:阅读理解

实验设计:
方法一:按照图1进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行。最终在___________容器中观察到白色沉淀,该实验中涉及的化学方程式有:_____________________________________________。
方法二:按图2进行实验,最终在两极间的溶液中首先观察到白色沉淀。请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl2溶液 ⑥乙醇 ⑦铁棒 ⑧植物油 ⑨碳棒
a___________,b___________,c___________,d___________。(填序号)
探究思考:实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)2如下信息:
资料名称 | 物理性质描述 | 化学性质描述 |
《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
《大学普通化学》(下册)傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3。这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+ |
阅读该资料后,你对上述实验中出现灰绿色或绿色的现象的解释是:______________________________;资料中提及的微绿色Fe3(OH)8,用氧化物的形式表示可写成______________________________。
(2)乙同学依据配色原理:白色和棕色不可能调配绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)2·nH2O所致。用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势。
加热时,“方法一”中弹簧夹C应处于_____________(填“打开”或“关闭”)状态,容器A中的反应须处于_____________(填“停止”或“发生”)状态。写出该实验中支持乙同学观点的化学方程式_________________________________________。
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe2+制备Fe(OH)2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释。你设计的方案为:_____________________。
查看答案和解析>>
科目: 来源: 题型:
A.测溶液pH的方法是:取一小片广泛pH试纸置于玻璃片或表面皿上,再用干燥、洁净的玻璃棒蘸取溶液,点在pH试纸中部,然后跟标准比色卡比较
B.在测定硫酸铜晶体结晶水含量的实验中,下列操作都会导致测定结果偏高:①加热前称量容器时,容器未完全干燥 ②加热过程中有少量晶体溅出 ③加热后容器未放入干燥器中冷却
C.配制0.1 mol·L-1的NaCl溶液250 mL,烧杯、玻璃棒、250 mL的容量瓶、胶头滴管等玻璃仪器必须用到
D.用50 mL酸式滴定管量取25.00 mL稀盐酸的操作可以是:先将稀盐酸注入酸式滴定管,调节其凹液面正好与25 mL该度相切,然后将溶液全部放入50 mL锥形瓶中
E.硝酸钾溶解度测定的实验中,温度计的水银球应处于烧杯中的水浴液面以下;分馏石油时,温度计的水银球应处于蒸馏烧瓶的支管口处
F.仪器洗涤中常采用下列方法:①用酒精清洗制取酚醛树脂用过的大试管 ②用氨水清洗做过银镜反应的试管 ③用浓盐酸稍加热清洗用高锰酸钾制氧气后的试管
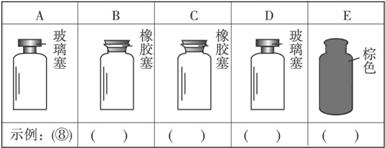
(2)实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下方的括号里:
①浓硫酸 ②碳酸钾溶液 ③碱石灰 ④四氯化碳 ⑤氯水 ⑥浓硝酸 ⑦硝酸银溶液 ⑧金属钠
查看答案和解析>>
科目: 来源: 题型:
A.1∶2 B.1∶1 C.5∶7 D.7∶5
查看答案和解析>>
科目: 来源: 题型:
A.若x=2,则p>0.5a B.若x=3,则p=![]() a
a
C.若x=4,则p=a D.若x=5,则p≥a
查看答案和解析>>
科目: 来源: 题型:
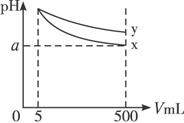
A.稀释后x溶液中水的电离程度比y溶液中水电离程度小
B.若x、y是一元碱,则等物质的量浓度的y的硝酸盐溶液的pH比x的硝酸盐溶液大
C.若x、y都是弱碱,则a的值一定大于9
D.完全中和x、y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y)
查看答案和解析>>
科目: 来源: 题型:
A.FeS2只作还原剂,CuSO4只作氧化剂
B.5 mol FeS2发生反应,有21 mol电子转移
C.产物中![]() 的离子都是氧化产物
的离子都是氧化产物
D.Cu2S既是氧化产物又是还原产物
查看答案和解析>>
科目: 来源: 题型:
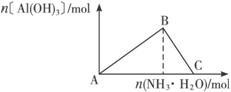
A.向AlCl3溶液中滴加氨水至过量
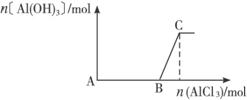
B.向NaOH溶液中滴入AlCl3溶液至过量且边滴边振荡

C.向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡
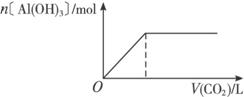
D.向NaAlO2溶液中缓缓通入二氧化碳至过量
查看答案和解析>>
科目: 来源: 题型:
A.溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2====2Fe3++2Br2+6Cl-
B.苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O![]() C6H5OH+
C6H5OH+![]()
C.铁屑溶于过量稀硝酸:3Fe+8H++2![]() ====3Fe2++2NO↑+4H2O
====3Fe2++2NO↑+4H2O
D.碳酸氢铵溶液与足量烧碱溶液反应:![]() +OH-====
+OH-====![]() +H2O
+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com