
科目: 来源: 题型:
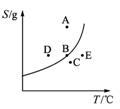
图1-1-3
(1)A、B、C三点的含义__________。
(2)A、B、C三点的溶质的质量分数的大小____________________。
(3)D、B、E三点的溶质的质量分数的大小____________________。
(4)将C点溶液变为饱和溶液应采取的措施是____________________。
查看答案和解析>>
科目: 来源: 题型:
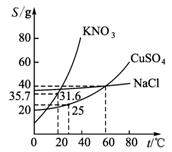
图1-1-2
A.40℃时,将35 g食盐溶于100 g水中,降温至0℃时,可析出NaCl晶体
B.20℃时KNO3饱和溶液的溶质质量分数为31.6%
C.60℃时,200 g水中溶解80 g CuSO4达饱和,当降温至30℃时,可析出30 g硫酸铜晶体
D.30℃时,将35 g KNO3和35 g NaCl同时溶于100 g水中,蒸发时先析出的晶体是NaCl
查看答案和解析>>
科目: 来源: 题型:
(1)此反应的化学方程式是(用NxHy表示)____________________________________。
(2)推算NxHy化学式的依据是_________。
(3)x与y的关系式为__________________。
查看答案和解析>>
科目: 来源: 题型:
A.X2气体过量 B.X2和Y2的体积均为50 mL
C.产物是双原子分子 D.无法判断
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解

NaCl晶体结构示意图
图1-1-1
(1)将固体NaCl细粒干燥后,准确称取m g NaCl固体并转移到定容仪器A中;
(2)用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积V cm3。
请回答下列问题:
①步骤(1)中A仪器最好使用__________ (填序号)。
A.量筒 B.烧杯 C.容量瓶 D.试管
②步骤(2)中用酸式滴定管还是用碱式滴定管__________,理由是____________________。
③能否用水代替苯__________,理由是___________________________________________。
④已知NaCl晶体中,靠得最近的Na+与Cl-间的平均距离为a cm(如图1-1-1),用上述测定方法测得的阿伏加德罗常数NA的表达式为_________________________________________。
(3)另一种方法是电解法,方法是:用铂电极电解CuCl2溶液时,当电流为I,通电时间为t(单位:分钟)时,阴极增加的质量为m,在阳极收集到气体体积(标准状况)为V。又知1个电子的电荷量为Q,铜的摩尔质量为M,则计算阿伏加德罗常数NA的算式为( )
A.It/QV B.32It/mQ C.672It/QV D.30MIt/mQ
(4)由实验得知,用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电量Q正比于金属的物质的量n和金属离子的化合价a的乘积,其比例系数F是一恒量,称为法拉第常数。它与金属的种类无关。
用电镀法在半径为R的铜球表面均匀镀上很薄的银层,在电解槽中铜球作__________极,另一电极材料是__________。若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d(用本题中的符号表示)。
查看答案和解析>>
科目: 来源: 题型:
(1)依题意判断,原溶液__________(填“是”或“不是”)饱和溶液;
(2)t℃下,该盐的溶解度为__________;
(3)若向原溶液中添加4.0 g溶质,则需要加入多少克水,才能使溶液恰好达到饱和。
查看答案和解析>>
科目: 来源: 题型:
(1)已知a g氧气中含有b个氧原子,则阿伏加德罗常数可表示为___________。
(2)已知标准状况下a L氧气中含有b个氧气分子,则阿伏加德罗常数可表示为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com